El impacto global del cáncer: prevención, detección y tratamientos actuales y emergentes
José Hernández Jiménez
2/4/202622 min leer



Introducción: el impacto global del cáncer
El cáncer continúa posicionándose como uno de los mayores desafíos para la salud en nuestra sociedad actual, siendo una de las causas principales de enfermedad y fallecimiento en todo el mundo. De hecho, si miramos los datos del año dos mil veintidós, las cifras son realmente impactantes: se diagnosticaron cerca de 20.000.000 de casos nuevos y se registraron más de 9.700.000 muertes a causa de esta patología. Estos números no son solo estadísticas; representan una carga sanitaria inmensa que afecta a todos los rincones del planeta.
¿Por qué siguen aumentando? Lo cierto es que las proyecciones globales apuntan a un crecimiento sostenido de la incidencia en los próximos años. Por un lado, esto se debe a que nuestra población vive más tiempo y el envejecimiento es un factor determinante en la aparición de tumores.
Sin embargo, no podemos ignorar que seguimos muy expuestos a factores de riesgo que, lejos de desaparecer, están aumentando en muchas regiones. Por cierto, hábitos como el consumo de tabaco, el incremento de la obesidad y la exposición constante a la contaminación ambiental son piezas clave que explican por qué el cáncer sigue ganando terreno.
Más allá de los informes médicos, el cáncer provoca una sacudida profunda que afecta a la estructura misma de nuestra sociedad. El golpe llega a las familias y pone a prueba la resistencia de los sistemas de salud.
De hecho, esta situación es especialmente preocupante en los países con menos recursos. En las naciones de ingresos bajos o medianos, el impacto económico es devastador porque, a menudo, los medios para lograr una detección temprana son insuficientes. Sin un diagnóstico a tiempo, las posibilidades de éxito del tratamiento disminuyen, agravando la crisis sanitaria en estas comunidades.
Al final, la lucha contra esta enfermedad no solo depende de la medicina, sino de cómo los países gestionan sus recursos. La falta de acceso a tecnologías de análisis y tratamiento en regiones vulnerables sigue siendo una de las grandes asignaturas pendientes. Reducir la mortalidad implica, necesariamente, mejorar la infraestructura sanitaria global para que el lugar donde nazca una persona no determine su capacidad de sobrevivir a un diagnóstico.
Datos de incidencia y mortalidad
A día de hoy, el cáncer supone una presión sanitaria a nivel mundial que no tiene comparación con casi ninguna otra patología. De hecho, si miramos las cifras publicadas en 2022 por la Organización Mundial de la Salud (OMS) mencionados anteriormente, se alcanzaron los 20.000.000 de nuevos diagnósticos, estimando un aumento de más de 35.000.000 nuevos casos para el año 2050. Esta cifra refleja la realidad que no deja de crecer el número de casos.
Dentro de este enorme volumen de casos, existen ciertas variantes que aparecen con muchísima más frecuencia que otras. Lo cierto es que los tumores de pulmón, mama y colorrectal se sitúan a la cabeza de las estadísticas globales.
Sin embargo, no son los únicos que mantienen en alerta a los sistemas de salud; el cáncer de próstata y el de estómago también se encuentran entre los más diagnosticados habitualmente. Por cierto, identificar estos patrones es fundamental para entender a qué nos enfrentamos como sociedad.
Lamentablemente, el impacto de la enfermedad no se mide solo en nuevos pacientes, sino también en las vidas que se pierden por el camino. En el mismo periodo analizado, los fallecimientos superaron los 9.700.000 muertes.
Esta cifra tan elevada es el reflejo de una lucha muy compleja. Por un lado, nos muestra lo difícil que resulta todavía tratar la enfermedad cuando se detecta en etapas avanzadas. Pero, por otro lado, evidencia una realidad incómoda: existen profundas desigualdades en el acceso a los cuidados médicos. De hecho, el éxito frente al cáncer no depende solo de la ciencia, sino de que los tratamientos efectivos puedan llegar a todas las personas por igual, sin importar dónde vivan.
Más allá de la estadística: Una realidad prioritaria en la salud global
Hablar de cáncer hoy en día es mucho más que analizar una estadística médica; es abordar una realidad que se ha vuelto prioritaria. De hecho, entender por qué esta enfermedad ocupa un lugar tan central nos ayuda a comprender mejor hacia dónde se dirige la salud global.
Lo primero que debemos notar es que la incidencia global de esta enfermedad no para de subir. Por cierto, este fenómeno está directamente relacionado con el hecho de que la sociedad está envejeciendo. Como ahora vivimos más años, la enfermedad ha adquirido una cronicidad que antes no era tan común, lo que obliga a los sistemas sanitarios a replantearse cómo cuidar a los pacientes a largo plazo.
Un punto realmente importante es que no estamos ante una batalla que dependa solo del azar. De hecho, existe un porcentaje muy alto de casos que se consideran prevenibles. Esto ocurre porque hay factores de riesgo modificables que, si logramos evitarlos o cambiarlos, podrían reducir drásticamente el número de diagnósticos. Al final, gran parte de la solución está en nuestras manos y en las políticas de prevención.
Afortunadamente, el panorama está cambiando gracias a las innovaciones constantes que están transformando la medicina. Los nuevos adelantos en la forma de realizar la detección y de aplicar la terapia están dando sus frutos. Estas mejoras tecnológicas prometen cambios muy positivos en los resultados de salud, permitiendo que los tratamientos sean cada vez más precisos y menos agresivos.
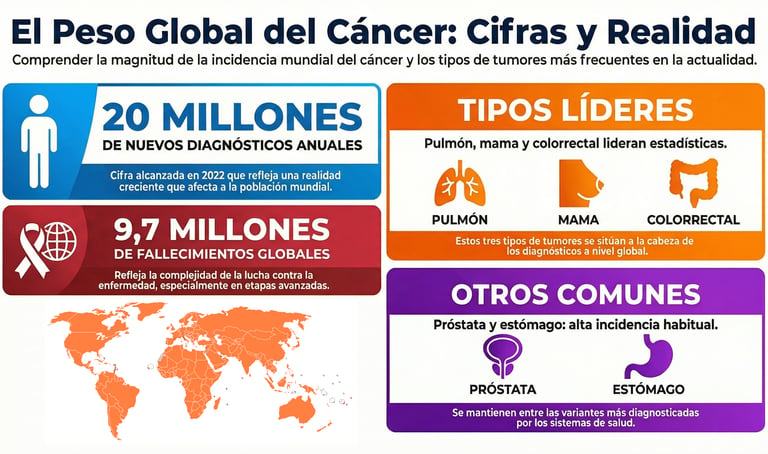
imagen: creación propia
Qué es el cáncer: biología esencial
Mutación celular y crecimiento descontrolado
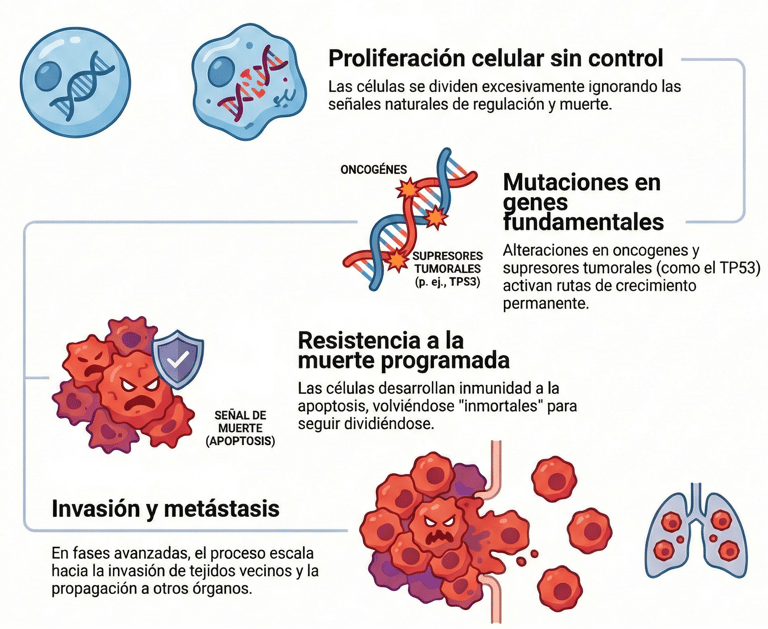
Lo primero que debemos entender es que el cáncer no es, en realidad, una única patología. De hecho, se trata de un conjunto de trastornos muy diversos que tienen algo en común: la proliferación incontrolada de un grupo de células transformadas. Estas unidades biológicas se vuelven rebeldes y consiguen saltarse a la torera todos los mecanismos que el cuerpo utiliza normalmente para regular cuánto deben crecer y en qué momento deben morir.
¿Cómo logran estas células tomar el control? Lo cierto es que este proceso comienza cuando se acumulan mutaciones en ciertos genes fundamentales, conocidos como oncogenes y supresores tumorales.
Al alterarse estos componentes, se activan de forma permanente las rutas de crecimiento y, lo que es peor, la célula desarrolla una resistencia a la apoptosis, que es el proceso de muerte programada que debería eliminarla. Sin embargo, al volverse "inmortales" y seguir dividiéndose, el problema escala hasta que, en fases más avanzadas, el cuerpo se enfrenta a la invasión de tejidos vecinos y a la temida metástasis.
Para comprender este avance, hay que poner el foco en los cambios genéticos y epigenéticos que impulsan la transformación hacia la malignidad. Por cierto, la ciencia ha identificado protagonistas muy claros en este escenario. Por ejemplo, es muy común encontrar fallos en el gen TP53, que actúa como un supresor tumoral vital, o ver cómo se producen amplificaciones en oncogenes como el HER2.
Además de estos genes específicos, el desarrollo de la enfermedad suele estar ligado a alteraciones en rutas de señalización críticas, como la vía PI3K/AKT/mTOR. Esta red de comunicación interna, cuando se estropea, contribuye tanto a que el tumor aparezca como a que progrese con mayor agresividad.
Al final, es este intrincado rompecabezas de señales químicas y errores en el ADN lo que define la progresión tumoral, convirtiendo un proceso biológico normal en un desafío sanitario de primer orden.
imagen: creación propia
Tipos más comunes
Si bien es cierto que el ser humano puede verse afectado por más de un centenar de variantes de esta enfermedad, lo cierto es que algunas de ellas aparecen con una frecuencia mucho mayor en las consultas médicas de todo el mundo. Esta realidad dibuja un mapa epidemiológico donde ciertos nombres se repiten con insistencia.
El cáncer de pulmón se sitúa, sin duda, a la cabeza de esta lista; no solo es el que más se diagnostica habitualmente, sino que también se ha convertido en el principal responsable de la mortalidad a nivel global. Por cierto, cuando ponemos el foco en la población femenina, es el cáncer de mama el que destaca por ser especialmente común.
De hecho, junto a estos, existen otros tipos de tumores que también muestran una incidencia muy elevada en diversas partes del mapa, como son el colorrectal, el de próstata y el de estómago.
Sin embargo, lo que hace que esta lucha sea tan difícil no es solo la cantidad de personas afectadas, sino la propia naturaleza de la enfermedad. Lo que llamamos cáncer es, en realidad, un fenómeno de una enorme heterogeneidad biológica.
Esto significa que estos tumores no son bloques uniformes, sino que presentan diferentes subtipos moleculares. Esta diversidad es la que explica por qué dos pacientes con el mismo diagnóstico pueden reaccionar de forma tan distinta; al final, esta complejidad es la que obliga a los médicos a buscar enfoques terapéuticos específicos para cada caso concreto.
Prevención del cáncer: ¿Qué podemos hacer nosotros?


imagen: creación propia
Factores de riesgo evitables
Lo cierto es que tenemos mucho más control del que imaginamos sobre esta enfermedad. Gran parte de los fallecimientos por cáncer están estrechamente vinculados a lo que los expertos llaman factores de riesgo modificables, es decir, elementos de nuestro estilo de vida y del medio ambiente que, en teoría, podríamos cambiar para protegernos mejor.
Hablamos de una proporción muy significativa de casos que podrían evitarse si prestamos atención a nuestro día a día. De hecho, llevar una dieta poco saludable, el consumo frecuente de alcohol o el problema de la obesidad son piezas clave en este rompecabezas. Por cierto, no todo depende de nuestras decisiones individuales; la contaminación ambiental también juega un papel fundamental y representa una carga importante para la salud pública actual.
Sin embargo, si hay un factor que destaca por encima de todos los demás por su capacidad de ser prevenido, ese es el tabaco. A día de hoy, sigue siendo el principal responsable de una gran variedad de diagnósticos oncológicos.
Es importante no bajar la guardia, ya que su impacto no se limita únicamente al sistema respiratorio. De hecho, además del cáncer de pulmón, el tabaquismo contribuye de forma decisiva al desarrollo de tumores en órganos como la vejiga y el páncreas. En definitiva, evitar este hábito sigue siendo la estrategia más potente que tenemos para reducir la mortalidad global.
Estilos de vida
Es fascinante cómo pequeñas decisiones cotidianas pueden cambiar drásticamente nuestro pronóstico de salud. Más allá de alejarse del tabaco, lo cierto es que nuestras costumbres pesan muchísimo; de hecho, elegir un estilo de vida saludable tiene la capacidad de recortar de forma considerable la aparición de los tumores más habituales.
Para que esto funcione, la clave está en el equilibrio: mantener una dieta equilibrada, asegurar una actividad física regular y, por cierto, vigilar que el consumo de alcohol sea siempre moderado. No se trata solo de "cuidarse", sino de reducir activamente la incidencia de cánceres comunes mediante hábitos que están bajo nuestro control.
Sin embargo, la protección no termina en lo que comemos o en cuánto nos movemos. La denominada prevención primaria cuenta hoy con un aliado tecnológico fundamental: las vacunaciones. De hecho, mucha gente se sorprende al saber que existen vacunas diseñadas específicamente para frenar cánceres virales.
En este sentido, las inmunizaciones dirigidas contra el Virus del Papiloma Humano y la hepatitis B han demostrado ser herramientas sumamente eficaces. Gracias a ellas, es posible evitar el desarrollo de enfermedades tan graves como el cáncer de cérvix y el hepatocelular. Al final, estas vacunas actúan como un escudo biológico que detiene la amenaza mucho antes de que el proceso maligno tenga oportunidad de comenzar.
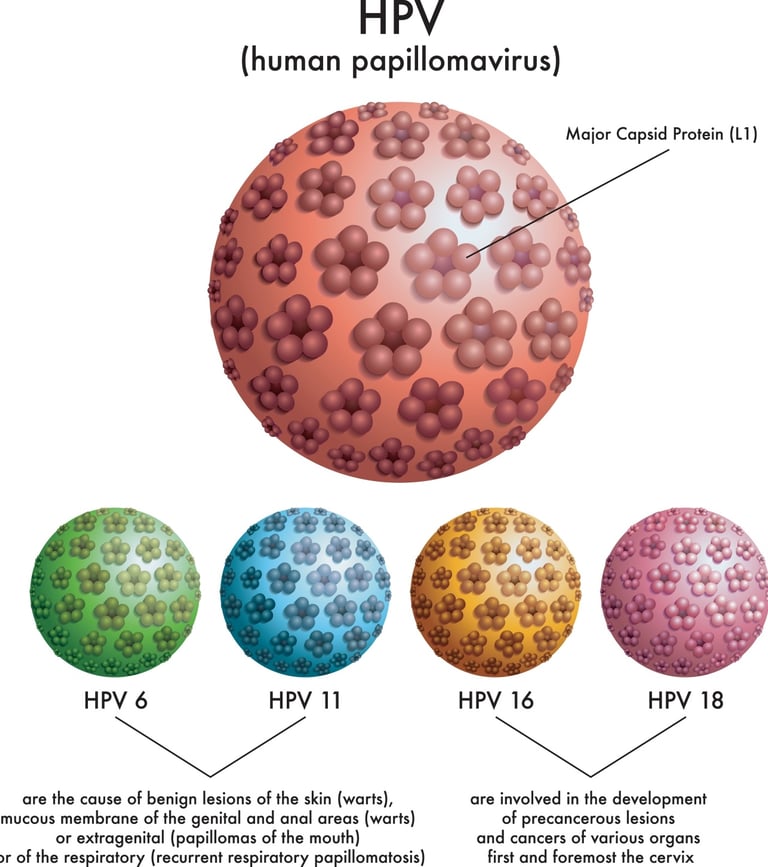
imagen: cookgyn.com
Detección temprana y cribado
Programas de screening
Identificar el cáncer en sus primeras fases es, sin duda, una de las herramientas más poderosas con las que cuenta la medicina moderna. De hecho, la detección temprana a través de programas de cribado organizados ha marcado un antes y un después en la lucha contra la enfermedad. Estos chequeos permiten localizar anomalías mucho antes de que se manifiesten los primeros síntomas clínicos, lo que cambia por completo el panorama para el paciente.
El éxito de este enfoque radica en encontrar la patología cuando todavía se encuentra en etapas tratables. Por ejemplo, herramientas como las mamografías para detectar el cáncer de mama, o las pruebas específicas para detectar la presencia del Virus del Papiloma Humano en el caso del cáncer cervical, son fundamentales. Por cierto, gracias a estas intervenciones, se ha logrado demostrar una mejora sustancial en la supervivencia, ya que permiten actuar en el momento preciso en que los tratamientos son más efectivos.
Sin embargo, para que estos resultados sean realmente masivos, es necesario que el cribado sistemático camine de la mano de políticas de salud pública bien estructuradas. No basta con tener la tecnología; lo que realmente marca la diferencia es la constancia y la organización de estos sistemas.
Al final, esta combinación de esfuerzos es lo que permite reducir drásticamente la mortalidad vinculada a tumores que son prevenibles o que, al menos, pueden atajarse en sus fases iniciales. Detectar a tiempo no es solo una opción médica, es la mejor estrategia para garantizar que la enfermedad no gane la batalla.
IA y nuevas tecnologías
No es ningún secreto que la tecnología está dando un giro radical a la medicina moderna. De hecho, la inteligencia artificial se ha convertido en una pieza fundamental para que la detección temprana sea mucho más eficaz, especialmente al refinar la forma en que los especialistas interpretan las imágenes de los pacientes y al optimizar los programas de cribado.
Sin duda, estas herramientas avanzadas están ayudando a exprimir al máximo el potencial de los sistemas de prevención. Por cierto, diversos análisis recientes han dejado claro que la aplicación de esta tecnología permite elevar la precisión diagnóstica de forma notable.
Lo que esto significa en el día a día es que se consiguen reducir los falsos positivos, evitando así que muchas personas pasen por el estrés de alarmas innecesarias en pruebas tan comunes como las mamografías y otras modalidades de detección sistemática.
Pero la innovación no se detiene en las imágenes externas. El uso de sistemas basados en machine learning está logrando avances que hace poco parecían inalcanzables. Por ejemplo, al aplicar estas técnicas de aprendizaje automático en las colonoscopias y otros exámenes diagnósticos, la capacidad para localizar lesiones precancerosas ha mejorado muchísimo.
Vaya por delante que el objetivo final es siempre adelantarse al problema. De hecho, encontrar tumores en etapas tempranas gracias a este apoyo tecnológico no solo facilita enormemente el trabajo de los médicos, sino que aumenta de forma drástica las probabilidades de éxito para los pacientes. Es, sencillamente, una nueva era para el diagnóstico médico.
Tratamientos actuales y emergentes: de dónde partimos y hacia dónde avanzamos
Cirugía, quimioterapia y radioterapia
Cuando nos enfrentamos a un diagnóstico de cáncer que todavía no se ha extendido, la cirugía suele ser, a día de hoy, la primera línea de defensa. Es el punto de partida habitual para retirar la masa principal. Sin embargo, no siempre es suficiente por sí sola.
De hecho, es muy común que los médicos decidan reforzar esta intervención con otros tratamientos adicionales. El objetivo es claro: barrer cualquier rastro de células tumorales residuales que haya podido quedar y, por cierto, reducir al máximo el riesgo de que la enfermedad vuelva a aparecer en el futuro.
Para lograr esta limpieza profunda, contamos con dos herramientas fundamentales que funcionan de maneras muy distintas. Por un lado, la quimioterapia realiza un trabajo de búsqueda y captura por todo el organismo, actuando de forma sistémica. Su especialidad es atacar a aquellas unidades biológicas que se dividen y crecen a toda velocidad, que es precisamente la característica principal de las células malignas.
Por otro lado, la radioterapia tiene un enfoque mucho más localizado. En lugar de recorrer todo el cuerpo, utiliza energía ionizante dirigida directamente sobre la zona afectada para provocar un daño celular letal en el corazón del tumor.
Aunque la medicina avanza a pasos agigantados, lo cierto es que estas técnicas siguen siendo esenciales. Sin embargo, no se limitan solo a un tipo de problema. Ambas estrategias continúan siendo los pilares básicos para el control de una gran variedad de procesos, desde los tumores sólidos más comunes hasta los diversos trastornos hematológicos que afectan a la sangre. Al final, combinar la precisión del bisturí con la potencia de los fármacos y la radiación es lo que permite ofrecer una respuesta sólida frente a la enfermedad.
Inmunoterapia e inhibidores de puntos de control
Estamos viviendo un cambio de era en la medicina, y la inmunoterapia es, sin duda, la gran protagonista de este siglo. A diferencia de los métodos tradicionales, esta técnica no ataca directamente al tumor, sino que "enseña" o entrena a nuestro propio sistema inmunitario para que sea él quien identifique y elimine a las células malignas. Es, básicamente, devolverle al cuerpo su capacidad de defensa.
Uno de los avances más potentes en este campo son los llamados inhibidores de puntos de control inmunitario. Seguro que les suenan nombres algo más técnicos como los anticuerpos anti-PD-1 y anti-CTLA-4.
De hecho, lo que hacen estas moléculas es algo fascinante: actúan como un interruptor que reinicia la respuesta inmunológica antitumoral. Gracias a este mecanismo, se ha logrado mejorar drásticamente la supervivencia en pacientes con diversos tipos de cánceres en etapas avanzadas, dándoles una oportunidad que antes parecía imposible.
Por otro lado, existen terapias todavía más sofisticadas, como la transferencia adoptiva de células T modificadas. Aquí es donde entran en juego tecnologías como el CAR-T y el TCR-T.
Sin embargo, aunque ya están mostrando resultados muy esperanzadores en casos de leucemias y en ciertos tumores sólidos, no hay que olvidar que su uso todavía se encuentra en una fase de expansión clínica. Es decir, es una vía con un potencial enorme, pero que aún se está perfeccionando para llegar a más gente.
Por cierto, uno de los grandes retos actuales de la ciencia es la precisión. No todos los organismos reaccionan igual, por lo que la investigación actual se está centrando con mucha fuerza en los predictores de respuesta.
El objetivo es sencillo de explicar, pero difícil de lograr: identificar de antemano qué pacientes obtendrán un beneficio real de estos tratamientos emergentes. Al final, se trata de personalizar la medicina para que cada persona reciba exactamente lo que su cuerpo necesita para ganar la batalla.
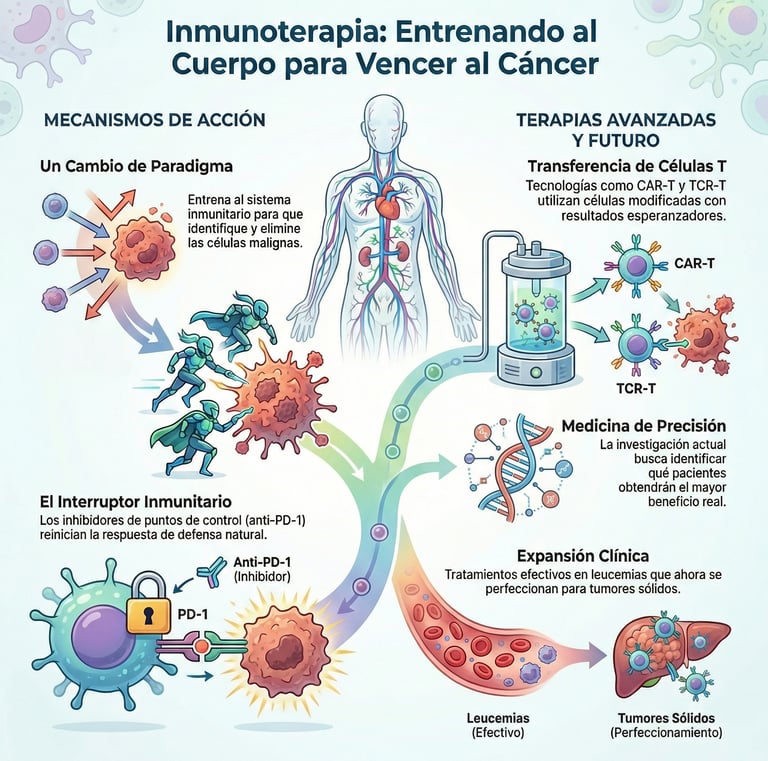
imagen: creación propia
Terapias dirigidas y medicina personalizada
El avance en el conocimiento sobre cómo funcionan los mecanismos moleculares que hacen crecer a un tumor ha cambiado las reglas del juego. Hoy en día, gracias a que entendemos mejor esos procesos internos, hemos podido diseñar las llamadas terapias dirigidas.
A diferencia de los métodos antiguos que atacaban a todas las células por igual, estas nuevas herramientas son mucho más selectivas. De hecho, contamos con fármacos capaces de bloquear señales de crecimiento muy concretas. Un gran ejemplo de esto es el targeting HER2 en el cáncer de mama, o el uso de inhibidores de tirosina quinasa, que actúan como francotiradores químicos sobre el objetivo.
Sin embargo, lo más emocionante es que ya no tratamos la enfermedad de forma genérica. Estamos entrando de lleno en la era de la medicina personalizada. ¿Qué significa esto en la práctica? Pues que ahora es posible realizar perfiles genómicos individuales de cada tumor para ver qué está pasando exactamente ahí dentro.
Al analizar las alteraciones genéticas específicas de cada paciente, los médicos pueden seleccionar el tratamiento que mejor se adapte a ese caso particular. Por cierto, esto no solo hace que las terapias sean mucho más efectivos, sino que también ayuda a que tengan una menor toxicidad, evitando efectos secundarios innecesarios.
En definitiva, ya no se trata de "probar suerte" con un tratamiento estándar. Lo que buscamos hoy es diseñar terapias a medida. Al final, entender el código genético del tumor nos permite atacar sus puntos débiles de forma directa y personalizada, marcando un antes y un después en la calidad de vida de las personas afectadas.
Derribando "barreras" a través de la ciencia: hallazgos del Dr. Mariano Barbacid en el cáncer de páncreas
El adenocarcinoma pancreático es, por desgracia, una de las formas más letales de cáncer que conocemos hoy en día. No solo es una enfermedad extremadamente agresiva en la clínica, sino que biológicamente se comporta de una manera totalmente distinta a otros tumores sólidos. De hecho, gran parte de su peligrosidad reside en un motor genético muy concreto: el oncogén KRAS.
Lo que ocurre en realidad es que este cáncer tiene una dependencia absoluta de las mutaciones en KRAS. Por cierto, este gen aparece alterado en más del 90% de los pacientes, presentándose principalmente en variantes específicas como G12D y G12V.
Estas mutaciones funcionan como un interruptor que se queda atascado en la posición de "encendido", activando de forma permanente rutas de crecimiento como MAPK/ERK y PI3K/AKT. Al final, esto no solo empuja a las células a multiplicarse sin descanso, sino que también les permite esquivar los mecanismos naturales de muerte celular programada.
Sin embargo, el papel de KRAS va mucho más allá de simplemente hacer crecer el tumor. Este gen es capaz de manipular el entorno que rodea a las células cancerosas para crear un microambiente inmunosupresor.
De hecho, lo que hace es reclutar células mieloides supresoras y bloquear las citocinas que deberían avisar a nuestras defensas para que ataquen. A través de diversos modelos genéticos, se ha podido comprobar que si logramos desactivar este gen, el tumor pierde gran parte de su capacidad para esconderse del sistema inmunitario. Por ejemplo, al eliminar la señal de KRAS, se reactivan mecanismos como los receptores de muerte celular Fas, facilitando que nuestras propias defensas hagan su trabajo.
En este escenario, el grupo liderado por el bioquímico Dr. Mariano Barbacid ha logrado un avance que ya se considera histórico. Utilizando modelos experimentales en ratones que replican fielmente las mutaciones humanas de KRAS y TP53, han podido ensayar estrategias que hasta hace poco parecían imposibles.
En un estudio publicado recientemente en una prestigiosa revista científica a finales de dos mil veinticinco, este equipo informó sobre una combinación triple de fármacos que ha logrado algo inédito: la regresión completa y duradera de los tumores.
La clave de este éxito ha sido dejar de lado la idea de usar un solo fármaco, algo que habitualmente provoca que el cáncer aprenda a defenderse rápido. En su lugar, han atacado tres puntos críticos a la vez:
Han utilizado un inhibidor experimental llamado daraxonrasib para bloquear directamente el gen mutado.
Han sumado un fármaco llamado afatinib para anular el receptor EGFR.
Finalmente, han incorporado un degradador de proteínas dirigido específicamente contra STAT3, conocido como SD36.
Esta estrategia conjunta consiguió detener la progresión de la enfermedad durante más de doscientos días en los modelos animales, sin que aparecieran señales de resistencia terapéutica ni toxicidad significativa. Vaya por delante que, aunque estos resultados son espectaculares y sugieren un potencial enorme, todavía no disponemos de evidencia en humanos.
Durante décadas, se pensó que la estructura de esta proteína era inexpugnable, casi como si fuera imposible de atacar con fármacos. No obstante, la aparición de inhibidores de tipo pan-KRAS y nuevas técnicas de degradación de proteínas están cambiando las reglas del juego.
El gran problema siempre ha sido que los tumores encuentran "vías de escape" a través de rutas alternativas como YAP1 o variantes de MEK/ERK. Por eso, el enfoque del bioquímico Dr. Mariano Barbacid es tan innovador: al bloquear toda la red de señales en lugar de un solo nodo, se le cierran todas las puertas al cáncer. Estamos, sin duda, ante uno de los avances más prometedores para entender y vencer la complejidad biológica de estos tumores.
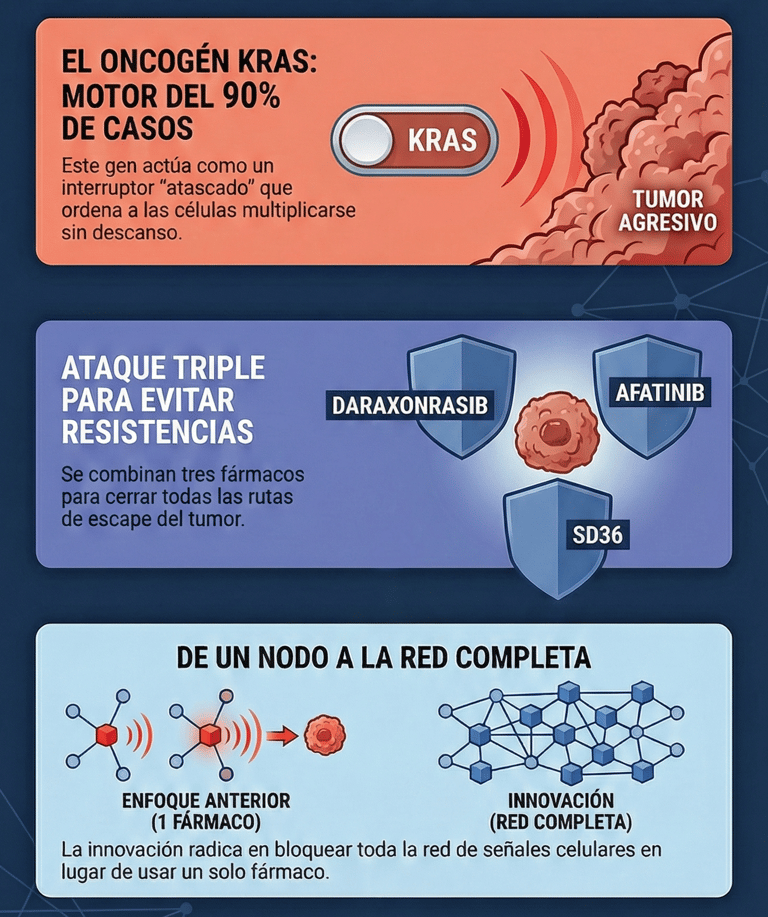
imagen: creación propia
Conclusión
A día de hoy, el cáncer se mantiene como uno de los desafíos más imponentes para la salud pública en todo el mundo. Lo cierto es que la incidencia de esta enfermedad no deja de crecer, impulsada en gran medida por los cambios demográficos, el entorno en el que vivimos y nuestros propios hábitos cotidianos. Es una realidad compleja, pero no todo son malas noticias.
A pesar de las cifras, estamos siendo testigos de un cambio de rumbo gracias a que ahora entendemos mucho mejor la biología de la enfermedad. De hecho, los avances en prevención primaria y los sistemas de cribado temprano están marcando la diferencia.
Sin embargo, lo que realmente ha revolucionado el panorama son los tratamientos innovadores. Herramientas como la inmunoterapia y las terapias dirigidas, sumadas al potencial de la inteligencia artificial, han dejado de ser promesas de futuro para convertirse en mejoras reales. Gracias a ellas, estamos viendo una evolución tangible tanto en la supervivencia como en la calidad de vida de muchísimos pacientes.
Finalmente, la investigación continua sigue siendo el motor de todo. Cada tumor es un mundo, y comprender esa biología y heterogeneidad es vital para seguir diseñando terapias de última generación. Lo cierto es que el cáncer de páncreas sigue posicionándose como uno de los desafíos más complicados para la medicina actual. Debido a su biología agresiva y a una asombrosa capacidad de resistencia terapéutica, esta enfermedad mantiene una supervivencia global lamentablemente baja. La clave de todo este proceso radica en la mutación de KRAS, que actúa como la auténtica piedra angular del tumor; por eso, gran parte de los esfuerzos científicos actuales se centran en ver cómo meterle mano a esa dependencia genética.
Sin embargo, no todo son sombras. Recientemente, el grupo liderado por el bioquímico Dr. Mariano Barbacid ha logrado un hito que ha sacudido el campo de la investigación preclínica. De hecho, han conseguido demostrar que una terapia dirigida combinada es capaz de eliminar el tumor de forma sostenida en modelos animales. Lo más llamativo es que lo han hecho sin que el cáncer aprenda a defenderse y sin que se aprecie una toxicidad evidente en los organismos estudiados. Es, sin duda, un avance espectacular en el laboratorio.
Ahora bien, hay que ser prudentes y tener los pies en el suelo. Aunque los resultados son brillantes, el salto hacia los ensayos clínicos con humanos todavía depende de obtener mucha más evidencia y de superar rigurosos procesos de validación. Por cierto, el camino que se abre ahora es fascinante. La idea es que, en los próximos años, el desarrollo de tratamientos que ataquen múltiples nodos de señalización del gen KRAS sea la norma.
Al final, la combinación de estas nuevas terapias con enfoques de tipo inmunológico y métodos de diagnóstico mucho más sensibles podría ser la clave definitiva. Estamos ante una patología que, históricamente, se ha mostrado muy rebelde ante los tratamientos convencionales, pero estos nuevos descubrimientos ofrecen una luz de esperanza real para cambiar su pronóstico en el futuro.
Sin duda, este descubrimiento es una de las señales más esperanzadoras que hemos visto en décadas contra el adenocarcinoma pancreático, un enemigo que siempre ha sido durísimo de pelar. Es un avance conceptual enorme: entender que la victoria no está en un solo fármaco, sino en desmantelar la red genética que protege al cáncer. Un hallazgo muy merecedor del Premio Nobel, siendo así sería el segundo bioquímico español en ser galardonado tras el bioquímico español Dr. Severo Ochoa.
Referencias:
1. Sung, H., Ferlay, J., Siegel, R. L., et al. (2024). Global cancer statistics 2024. CA: A Cancer Journal for Clinicians, 74(1), 9–34. https://pubmed.ncbi.nlm.nih.gov/
2. Bray, F., Laversanne, M., Weiderpass, E., & Soerjomataram, I. (2024). The ever-increasing importance of cancer. The Lancet, 403, 1045–1047. https://pubmed.ncbi.nlm.nih.gov/
3. Miller, K. D., et al. (2023). Cancer statistics, 2023. CA: A Cancer Journal for Clinicians, 73(1), 17–48. https://pubmed.ncbi.nlm.nih.gov/
4. Wild, C. P., Weiderpass, E., & Stewart, B. W. (2023). World Cancer Report. IARC/WHO. https://pubmed.ncbi.nlm.nih.gov/
5. Sung, H., et al. (2023). Global patterns in cancer survival. The Lancet Oncology, 24, 1–15. https://pubmed.ncbi.nlm.nih.gov/
6. Hanahan, D. (2022). Hallmarks of cancer: New dimensions. Cancer Discovery, 12(1), 31–46.
7. Vogelstein, B., et al. (2023). Cancer genome landscapes revisited. Science, 380, eabm3433.
8. Greaves, M., & Maley, C. C. (2022). Clonal evolution in cancer. Nature, 481, 306–313.
9. Stratton, M. R., Campbell, P. J., & Futreal, P. A. (2022). The cancer genome. Nature, 458, 719–724.
10. Bedard, P. L., et al. (2022). Tumour heterogeneity. Nature, 501, 355–364.
11. Siegel, R. L., et al. (2023). Cancer trends by tumor type. CA, 73, 233–254.
12. Alexandrov, L. B., et al. (2022). Mutational signatures. Nature Reviews Cancer, 22, 1–19.
13. Dienstmann, R., et al. (2022). Precision oncology taxonomy. Nat Rev Clin Oncol, 19, 1–18.
14. Islami, F., et al. (2024). Cancer cases attributable to modifiable risk factors. CA, 74, 89–112.
15. Vineis, P., & Wild, C. P. (2022). Global cancer prevention. Nat Rev Cancer, 22, 1–14.
16. Brawley, O. W. (2022). Risk-based prevention. JAMA, 327, 2277–2278.
17. Loomis, D., et al. (2023). Environmental carcinogens. The Lancet Oncology, 24, 1–12.
18. Key, T. J., et al. (2022). Diet, obesity and cancer. Nat Rev Cancer, 22, 1–15.
19. Rehm, J., et al. (2023). Alcohol consumption and cancer. The Lancet Oncology, 24, 1–10.
20. Moore, S. C., et al. (2022). Physical activity and cancer risk. JAMA Oncology, 8, 1–9.
21. US Preventive Services Task Force. (2023). Cancer screening recommendations. JAMA.
22. Bretthauer, M., et al. (2023). Benefits and harms of screening. The Lancet, 401, 128–140.
23. Tabár, L., et al. (2022). Breast cancer screening outcomes. Radiology, 302, 1–10.
24. Imperiale, T. F., et al. (2023). Colorectal screening strategies. NEJM, 389, 1–11.
25. Topol, E. J. (2024). Artificial intelligence in medicine. Nature Medicine, 30, 1–10.
26. Esteva, A., et al. (2023). Deep learning in healthcare. Nature Medicine, 29, 1–12.
27. McKinney, S. M., et al. (2022). AI in breast cancer screening. Nature, 577, 89–94.
28. Kather, J. N., et al. (2022). AI-based pathology. Nat Rev Cancer, 22, 1–12.
29. Conroy, T., et al. (2022). Neoadjuvant therapy in rectal cancer. NEJM, 386, 1343–1355.
29. Early Breast Cancer Trialists’ Collaborative Group. (2023). Chemotherapy outcomes. The Lancet, 401, 1–12.
30. Delaney, G., et al. (2022). Radiotherapy effectiveness. Lancet Oncology, 23, 1–10.
32. Sharma, P., & Allison, J. P. (2023). Checkpoint inhibitors. Science, 381, eadd7987.
33. Ribas, A., & Wolchok, J. D. (2022). Cancer immunotherapy. Science, 359, 1350–1355.
34. Zitvogel, L., et al. (2023). Immunotherapy overview. Immunity, 56, 219–236.
35. June, C. H., et al. (2022). CAR-T cell therapy. Science, 359, 1361–1365.
36. Drilon, A., et al. (2023). Targeting oncogenic drivers. JCO, 41, 971–985.
37. André, F., et al. (2022). PIK3CA-mutated breast cancer. NEJM, 380, 1929–1940.
38. Baselga, J., & Swain, S. M. (2023). Targeted therapies. Nat Rev Cancer, 23, 1–14.
39.Tsimberidou, A. M., et al. (2022). Precision oncology trials. JCO, 40, 1–10.
40. Vasan, N., et al. (2022). Mechanisms of resistance. Nature, 575, 299–309.
41.McGranahan, N., & Swanton, C. (2022). Clonal diversity. Cell, 168, 613–628.
42. Nekhlyudov, L., et al. (2023). Cancer survivorship. CA, 73, 1–24.
43. Bluethmann, S. M., et al. (2022). Long-term survivorship. JNCI, 114, 1–9.
44. Farmer, P., et al. (2023). Global cancer equity. The Lancet, 401, 1–12.
45.Atun, R., et al. (2022). Cancer care systems. The Lancet Oncology, 23, 1–11
46.Liaki V, Barrambana S., et al. (2025). A targeted combination therapy achieves effective pancreatic cancer regression and prevents tumor resistance. Proc Natl Acad Sci U S A. 9;122(49)
47.Ballesteros-González I, Hernández-Navas I. et al. (2025). The repressor Capicua is a barrier to lung tumor development driven by Kras/Trp53 mutations. EMBO Mol Med. 17(12):3377-3406.
48.Drosten M, Barbacid M. (2025). The rapidly growing landscape of RAS inhibitors: from selective allele blockade to broad inhibition strategies. Mol Oncol. 19(11):2991-2995.