Enfermedades raras: De la odisea diagnóstica a la revolución genómica
José Hernández Jiménez
2/28/202612 min leer


Introducción
¿Qué entendemos realmente por enfermedad rara?
Lo cierto es que las enfermedades raras forman un grupo increíblemente diverso de trastornos que, a primera vista, parecen casos aislados. Aunque cada una de ellas se da en muy poquitas personas, si las miramos en su conjunto, nos damos cuenta de que representan un desafío enorme para la salud en todo el mundo. De hecho, no hay una única forma de definirlas, ya que los criterios cambian según la zona geográfica y sus leyes.
Sin embargo, por citar dos ejemplos claros, en la Unión Europea se considera que una patología es rara cuando su prevalencia es menor de cinco casos por cada diez mil personas. Por otro lado, en Estados Unidos el listón se pone en que haya menos de doscientas mil personas afectadas en todo el país.
El peso de la genética en los más jóvenes
A pesar de que se han identificado miles de estas patologías, la gran mayoría comparte algo fundamental: su origen genético. Lo habitual es que estas condiciones den la cara muy pronto, casi siempre en los primeros años de vida, y que no se queden en un solo órgano, sino que afecten a varios sistemas a la vez. Esto acaba provocando situaciones de discapacidad, problemas de comorbilidad entre otros. Al final, no es solo el paciente quien la sufre; de hecho, toda la familia se ve profundamente afectada por el impacto de la enfermedad.
Cómo se definen y cuántas existen
El "laberinto" de las definiciones
Si buscamos una definición única y universal para lo que es una enfermedad rara, lo cierto es que no la vamos a encontrar. De hecho, aunque casi todo el mundo se guía por la prevalencia poblacional para identificarlas, los criterios cambian bastante dependiendo de la frontera que crucemos. Sin embargo, lo más habitual es que los marcos legales y de salud pública establezcan umbrales muy variados; por cierto, estos pueden oscilar desde un caso por cada dos mil personas hasta uno por cada doscientas mil, según el país o la región en la que nos encontremos.
Un catálogo inmenso en constante expansión
Por otro lado, la cantidad de condiciones distintas que se han descrito hasta hoy es realmente abrumadora. Actualmente, se estima que existen entre siete mil y diez mil enfermedades diferentes, y la gran mayoría de ellas aparecen reportadas en bases de datos especializadas como Orphanet o GeneMap.
Es verdad que estas cifras pueden variar a medida que la ciencia hace nuevos descubrimientos, pero lo que nadie pone en duda es la enorme heterogeneidad diagnóstica de estas afecciones. Al final, nos enfrentamos a miles de entidades clínicas y moleculares distintas, lo que hace que cada caso sea un mundo.
La genética como pieza clave
Si rascamos un poco en la raíz de este desafío, la evidencia molecular nos indica que la gran mayoría de estas patologías tiene un origen genético. Precisamente por este motivo, la genómica ha pasado a ocupar un lugar central. Hoy en día, no se entiende la caracterización y diagnóstico de estas enfermedades sin el apoyo de esta disciplina, que es la que nos permite entender qué está pasando realmente a nivel biológico en cada paciente.
Epidemiología
La paradoja de lo que llamamos "raro"
A veces los términos nos confunden: aunque solemos pensar que una enfermedad rara es algo aislado, la realidad colectiva es muy distinta. De hecho, si bien cada una de estas patologías afecta a un grupo muy reducido de personas, cuando las sumamos todas, nos damos cuenta de que impactan a un porcentaje altísimo de la sociedad. Es curioso, pero lo que es poco común de forma individual se convierte en un reto de salud masivo a nivel global
Millones de personas bajo el mismo paraguas
Si miramos los números, la magnitud del problema se hace evidente. Según diversos estudios realizados en todo el mundo, se calcula que entre el 3,5 % y el 5,9 % de la población mundial podría convivir con alguna de estas afecciones en algún momento de su vida. Por cierto, esto no es una cifra menor; estamos hablando de cientos de millones de personas en todo el planeta que comparten esta realidad.
Estos datos no surgen de la nada. Provienen de análisis minuciosos en bases de datos globales especializadas, donde se registran miles de condiciones diferentes cuyas tasas de prevalencia cambian drásticamente dependiendo de la patología específica que estemos analizando.
Por qué son tan difíciles de diagnosticar
Una "travesía" llena de obstáculos
Ponerse en la piel de alguien que busca respuestas sobre su salud no siempre es fácil, y menos cuando se trata de una patología poco común. Conseguir ponerle nombre a lo que te pasa se convierte, muy a menudo, en lo que llamamos una odisea diagnóstica. De hecho, hablamos de un camino agotador de consultas interminables y pruebas constantes que pueden alargarse durante años. Sin embargo, no es hasta que se alcanza un diagnóstico molecular definitivo cuando los pacientes y sus familias encuentran, por fin, algo de luz en ese proceso.
Por qué la biología nos lo pone difícil
¿Pero por qué es tan complicado dar en el clavo? Para empezar, nos topamos con la heterogeneidad fenotípica. Esto significa, básicamente, que un mismo gen puede manifestarse de formas totalmente distintas en cada persona, lo que impide que existan patrones de diagnóstico claros y fáciles de seguir.
A esto hay que sumarle la baja prevalencia de estas condiciones. Como son casos tan poco frecuentes, es muy difícil que el personal médico esté familiarizado con ellos. Por cierto, esa falta de contacto habitual con la enfermedad limita mucho que los profesionales puedan acumular la experiencia clínica necesaria para identificarlas con rapidez.
La tecnología no llega a todos por igual
Aunque hoy en día la secuenciación del genoma completo está revolucionando la medicina, nos enfrentamos a un problema de equidad. El acceso a estas tecnologías de vanguardia no es uniforme en todo el mundo. De hecho, esta desigualdad se ha convertido en una barrera global que deja a muchísimos pacientes fuera del sistema, impidiéndoles beneficiarse de los últimos avances en genómica.
Un rayo de esperanza en momentos críticos
Sin embargo, no todo son malas noticias. Investigaciones recientes han dado un vuelco a la situación, especialmente en las unidades de cuidados intensivos pediátricos. Se ha demostrado que, si se utiliza la secuenciación genómica de manera rápida, el tiempo para obtener un resultado se reduce drásticamente: pasamos de esperar años a tener respuestas en solo unos días. Este avance es fundamental, ya que conseguir un diagnóstico veloz permite tomar decisiones clínicas que pueden cambiar por completo el futuro del paciente.
Ejemplos representativos de enfermedades raras
Para comprender realmente la inmensa variedad de las enfermedades poco frecuentes, no hay nada mejor que detenerse en algunos casos específicos que, por su naturaleza, nos muestran lo complejo que puede ser el cuerpo humano. Lo cierto es que estas patologías no siguen un único patrón, sino que forman un mosaico de síntomas y causas muy diversas.
Un vistazo a la diversidad de los trastornos
Por ejemplo, hablemos de la ataxia telangiectasia. Se trata de un trastorno neurodegenerativo que afecta directamente al cerebelo, provocando alteraciones en el movimiento. Pero la cosa no queda ahí; de hecho, quienes conviven con esta condición suelen tener una predisposición a infecciones y un riesgo mayor de desarrollar cáncer. Es un recordatorio de cómo un solo problema genético puede afectar a múltiples sistemas del organismo.
Sin embargo, existen otros casos igualmente complejos, como el síndrome de Hermansky Pudlak. En este caso, estamos ante una enfermedad autosómica recesiva que se manifiesta principalmente a través del albinismo y ciertos defectos plaquetarios. Es fascinante, y a la vez preocupante, cómo una alteración en la sangre y la pigmentación pueden ir de la mano de esta manera tan específica.
Casos de una escasez extrema
Si nos adentramos en lo que podríamos llamar "lo más raro entre lo raro", nos topamos con el síndrome del neurodesarrollo de Okur Chung. Por cierto, esta es una condición extremadamente rara donde los síntomas principales son el retraso en el desarrollo y trastornos significativos en el lenguaje. Al ser tan inusual, cada caso diagnosticado es una pieza clave para la ciencia.
Aún más impactante es el síndrome de aplasia fibular y ectrodactilia. Aquí hablamos de una anomalía genética del desarrollo esquelético que tiene una frecuencia de aparición bajísima, de hecho, afecta a menos de una de cada millón de personas. La singularidad de este tipo de trastornos óseos es un claro ejemplo de los desafíos a los que se enfrenta la medicina actual.
Una mínima parte de un universo inmenso
Al final, estos ejemplos son solo una pequeñísima muestra de todas las patologías que se han descrito hasta el momento. La realidad es que el catálogo de enfermedades raras es gigantesco y abarca desde trastornos metabólicos hasta síndromes congénitos complejos. Ninguna historia clínica es igual a otra, y esa es precisamente la razón por la que la investigación personalizada es tan necesaria hoy en día.
Investigación, terapias innovadoras y medicina personalizada
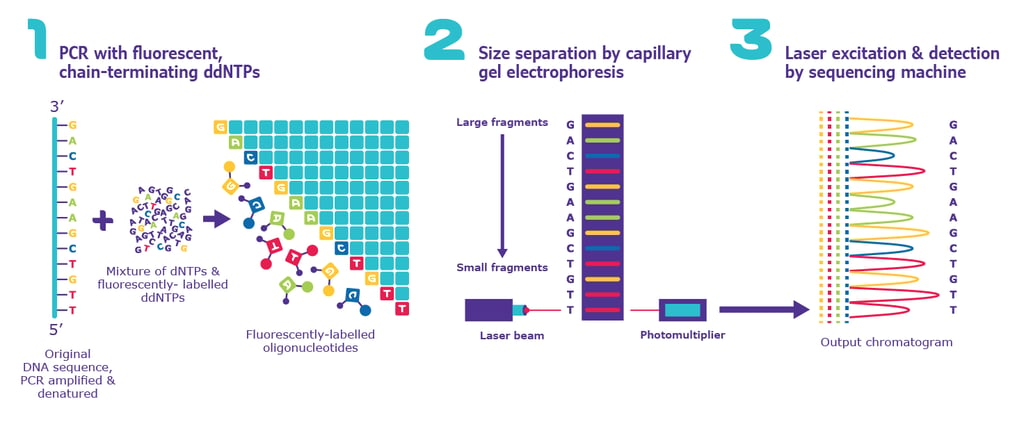
imagen: sigmaaldrich.com
La gran revolución en el laboratorio
La forma en que investigamos las enfermedades poco frecuentes ha dado un giro espectacular últimamente. De hecho, gracias a la evolución de la genómica, a las nuevas formas de analizar la información y al auge de la medicina personalizada, estamos en una etapa totalmente distinta. Por cierto, las herramientas de secuenciación del exoma y la secuenciación del genoma completo han demostrado ser increíblemente eficaces. Lo que las hace especiales es su capacidad para rastrear y localizar variantes patogénicas incluso en las regiones no codificantes del genoma, esas zonas del ADN que antes eran un misterio para nosotros pero que ahora sabemos que guardan respuestas clave.
Hacia una medicina hecha a medida
Pero no se trata solo de obtener datos, sino de saber qué hacer con ellos. Sin embargo, lo que realmente está marcando la diferencia es cómo estamos empezando a integrar los modelos clínico genómicos en la práctica diaria de los diagnósticos. Actualmente, se están diseñando enfoques algorítmicos personalizados con un objetivo muy claro: adaptar los tratamientos a las necesidades moleculares específicas de cada persona. Al final, esta unión entre la información genética y el uso inteligente de algoritmos es lo que nos permite ser mucho más precisos a la hora de detectar una enfermedad y, sobre todo, al elegir el tratamiento adecuado.
Descubriendo puentes entre enfermedades
Además, hay algo fascinante que está ocurriendo gracias a la mezcla de los datos genéticos con la inteligencia artificial y el análisis de grandes volúmenes de información, lo que conocemos como big data. De hecho, esta combinación está acelerando muchísimo la velocidad a la que descubrimos nuevos mecanismos patogénicos. Lo mejor de todo es que este enfoque nos ayuda a ver que enfermedades que parecen distintas podrían compartir patrones internos. Esto abre una puerta de esperanza enorme, ya que nos permite identificar posibles tratamientos que se dirijan a esos patrones moleculares comunes, beneficiando a pacientes de diferentes patologías a la vez.
Conclusión
Aunque a veces se piensa en ellas como casos aislados, lo cierto es que las patologías poco frecuentes forman un grupo de condiciones clínico-genéticas increíblemente variado. Por separado parecen pocas, pero si las sumamos, la realidad es que afectan a cientos de millones de personas en todo el mundo. Es curioso cómo algo que llamamos "raro" puede ser, colectivamente, tan masivo.
De hecho, aunque el número exacto de estas enfermedades y su definición varían según las leyes de cada país, hay un punto de unión indiscutible: su base genética. Por este motivo, hoy en día es impensable mejorar su manejo o su detección sin poner las estrategias de secuenciación y la genómica en el centro de la mesa. Sin estas herramientas, estaríamos a ciegas.
Sin embargo, no todo es tan sencillo. Uno de los grandes muros con los que nos topamos es la epidemiología. Sigue siendo un reto tremendo entender el alcance real de estas dolencias porque no existen datos uniformes en todas las regiones del planeta. Aun así, con lo que sabemos ahora, está claro que deben ser una prioridad absoluta en la salud pública.
Muchos pacientes se ven atrapados en lo que se conoce como la odisea diagnóstica, un laberinto que puede durar años. Por suerte, esto está empezando a cambiar para mejor. Gracias a la implementación de tecnologías genómicas rápidas y personalizadas, estamos logrando acortar esos tiempos y ofrecer respuestas mucho antes.
De cara al futuro, el panorama es esperanzador. Los saltos que estamos dando en medicina personalizada y en el desarrollo de herramientas analíticas de precisión tienen la capacidad de darle un vuelco total a la atención médica.
No se trata solo de ponerle nombre a la enfermedad con mayor exactitud, que ya es mucho, sino de abrir la puerta a tratamientos dirigidos. La idea es atacar el problema basándose en los mecanismos moleculares específicos de cada individuo. En definitiva, estamos pasando de una medicina generalista a una que entiende y respeta la particularidad biológica de cada paciente.

Referencias
Abbas, S. R., Abbas, Z., Zahir, A., & Lee, S. W. (2025). Advancing genome-based precision medicine: A review on machine learning applications for rare genetic disorders. Briefings in Bioinformatics, 26(4), bbaf329. https://doi.org/10.1093/bib/bbaf329
Ali, S. S., Li, Q., & Agrawal, P. B. (2025). Implementation of multi-omics in diagnosis of pediatric rare diseases. Pediatric Research, 97(4), 1337–1344. https://doi.org/10.1038/s41390-024-03728-w
Berrocal-Acedo, M., Benito-Lozano, J., Alonso-Ferreira, V., & Vilches-Arenas, Á. (2022). Retraso diagnóstico en enfermedades raras: revisión sistemática. Revista Española de Salud Pública, 96, e202201001. https://ojs.sanidad.gob.es/index.php/resp/article/view/347
Cortés, F. M. (2022). Medicina de precisión de enfermedades raras. Revista Médica Clínica Las Condes, 33(2), 148-153. https://doi.org/10.1016/j.rmclc.2022.03.005
Hartley, T., Gillespie, M. K., Graham, I. D., Hayeems, R. Z., Li, S., Sampson, M., Boycott, K. M., & Potter, B. K. (2023). Exome and genome sequencing for rare genetic disease diagnosis: a scoping review and critical appraisal of clinical guidance documents produced by genetics professional organizations. Genetics in Medicine, 25(11), 100948. https://doi.org/10.1016/j.gim.2023.100948
Hermida-Ameijeiras, Á. (2024). Special Issue “Diagnosis and Treatment of Rare Diseases”. Journal of Clinical Medicine, 13(9), 2574. https://doi.org/10.3390/jcm13092574
Hong, J., Lee, D., Hwang, A., Kim, T., Ryu, H.-Y., & Choi, J. (2024). Rare disease genomics and precision medicine. Genomics & Informatics, 22, 28. https://doi.org/10.1186/s44342-024-00032-1
Larizza, L., & Cubellis, M. V. (2023). Rare diseases: Implementation of molecular diagnosis, pathogenesis insights and precision medicine treatment. International Journal of Molecular Sciences, 24(10), 9064. https://doi.org/10.3390/ijms24109064
Mackley, M. P., et al. (2025). Genomic sequencing technologies for rare disease in mainstream healthcare: the current state of implementation. European Journal of Human Genetics, 33(11), 1402-1413. https://doi.org/10.1038/s41431-025-01925-7
Méndez-Vidal, C., Bravo-Gil, N., Pérez-Florido, J., Marcos-Luque, I., Fernández, R. M., Fernández-Rueda, J. L., & Antiñolo, G. (2025). A genomic strategy for precision medicine in rare diseases: Integrating customized algorithms into clinical practice. Journal of Translational Medicine, 23, 86. https://doi.org/10.1186/s12967-025-06069-2
Pagnamenta, A. T., Camps, C., Giacopuzzi, E., Taylor, J. M., Hashim, M., Calpena, E., … Vavoulis, D. V. (2023). Structural and non-coding variants increase the diagnostic yield of clinical whole genome sequencing for rare diseases. Genome Medicine, 15(94). https://doi.org/10.1186/s13073-023-01240-0
Pitsava, G., Hawley, M., Auriga, L., et al. (2025). Genome sequencing reveals the impact of pseudoexons in rare genetic disease. Genetics in Medicine, 27(11), 101574. https://doi.org/10.1016/j.gim.2025.101574
Prevalence data summary from rare disease epidemiology. Estimated >7,000 distinct rare diseases in total, with ~4 % lifetime population prevalence. (Epidemiological estimates from scientific sources).
Schobers, G., Derks, R., den Ouden, A., Swinkels, H., van Reeuwijk, J., Bosgoed, E., … Vissers, L. E. L. M. (2024). Genome sequencing as a generic diagnostic strategy for rare disease. Genome Medicine, 16, 32. https://doi.org/10.1186/s13073-024-01301-y
Stark, J. C., Pipko, N., Liang, Y., & others. (2025). Clinical applications of and molecular insights from RNA sequencing in a rare disease cohort. Genome Medicine, 17, 72. https://doi.org/10.1186/s13073-025-01494-w
Tesi, B., Boileau, C., Boycott, K. M., Canaud, G., Caulfield, M., Choukair, D., … Lindstrand, A. (2023). Precision medicine in rare diseases: what is next? Journal of Internal Medicine, 294(4), 397–412. https://doi.org/10.1111/joim.13655
Thorpe, E., Williams, T., Shaw, C., Chekalin, E., Ortega, J., Robinson, K., … Taft, R. J. (2024). The impact of clinical genome sequencing in a global population with suspected rare genetic disease. American Journal of Human Genetics, 111(7), 1271-1281. https://doi.org/10.1016/j.ajhg.2024.05.006
Wilke, M. V. M. B., Klee, E. W., Dhamija, R., … (2024). Diagnostic yield of exome and genome sequencing after non-diagnostic multi-gene panels in patients with single-system diseases. Orphanet Journal of Rare Diseases, 19, 216. https://doi.org/10.1186/s13023-024-03213-x
Wojcik, M. H., Lemire, G., Berger, E., Zaki, M. S., Wissmann, M., Win, W., … Place, E. M. (2024). Genome sequencing for diagnosing rare diseases. New England Journal of Medicine, 390(21), 1985–1997. https://doi.org/10.1056/NEJMoa2314761