Paludismo: la enfermedad que el mundo aún no ha eliminado
José Hernández Jiménez
4/24/202617 min leer
Introducción
Aunque vivamos en una era de avances tecnológicos constantes, el paludismo —que muchos conocemos simplemente como malaria— sigue siendo a día de hoy uno de los mayores quebraderos de cabeza para la salud pública global. Es una de esas enfermedades infecciosas que, por mucho que investiguemos, se resiste a desaparecer de nuestro mapa biomédico.
A decir verdad, el panorama actual es bastante serio. A pesar de que llevamos décadas lanzando campañas de prevención y buscando nuevas terapias, las cifras no mienten: esta enfermedad todavía se cobra cientos de miles de vidas cada año, cebándose especialmente con las regiones más vulnerables del planeta.
De hecho, los datos del año 2024 son un toque de atención para todos. Se estima que hubo unos 282 millones de casos y que las muertes superaron las 600.000. Lo más preocupante, sin embargo, es que desde mediados de la década pasada parece que nos hemos estancado; los avances globales no terminan de arrancar y la situación se siente algo bloqueada.
Pero, ¿por qué es tan difícil de frenar? La culpa la tiene un parásito del género Plasmodium, que llega a nosotros a través de la picadura de mosquitos infectados, concretamente del género Anopheles. No es solo una cuestión de biología pura y dura, que ya de por sí es enrevesada.
Al final, la lucha se complica por una mezcla de factores sociales, económicos y ambientales que históricamente han entorpecido cualquier intento de erradicación. Por si fuera poco, nos enfrentamos a un reto creciente: la aparición de resistencias farmacológicas y también vectoriales. Básicamente, tanto el parásito como el mosquito están aprendiendo a "esquivar" nuestras medicinas y las herramientas que usamos para controlarlos.
Por cierto, no todo son noticias desalentadoras. En los últimos años hemos sido testigos de lo que podríamos llamar un auténtico hito en la historia de la medicina. Por fin se han desarrollado las primeras vacunas eficaces contra un parásito humano, las denominadas RTS,S y R21.
Sin duda, esto marca un antes y un después. Sin embargo, estos logros científicos tan brillantes tienen que convivir con una realidad mucho más cruda: las profundas desigualdades estructurales. Mientras existan estas brechas, la transmisión de la enfermedad encontrará siempre un resquicio donde perpetuarse, recordándonos que la ciencia, por sí sola, necesita de la equidad para ser realmente transformadora.
¿Qué es el paludismo y cómo actúa en el cuerpo?
El paludismo es una enfermedad infecciosa causada por protozoos del género Plasmodium, de los cuales cinco especies afectan al ser humano: P. falciparum, P. vivax, P. ovale, P. malariae y P. knowlesi. Entre ellas, P. falciparum es responsable de la mayor mortalidad global, mientras que P. vivax destaca por su amplia distribución geográfica y su capacidad de causar recaídas debido a formas latentes hepáticas. La infección se transmite exclusivamente a través de la picadura de mosquitos hembra del género Anopheles, lo que convierte al paludismo en una enfermedad vectorial compleja.
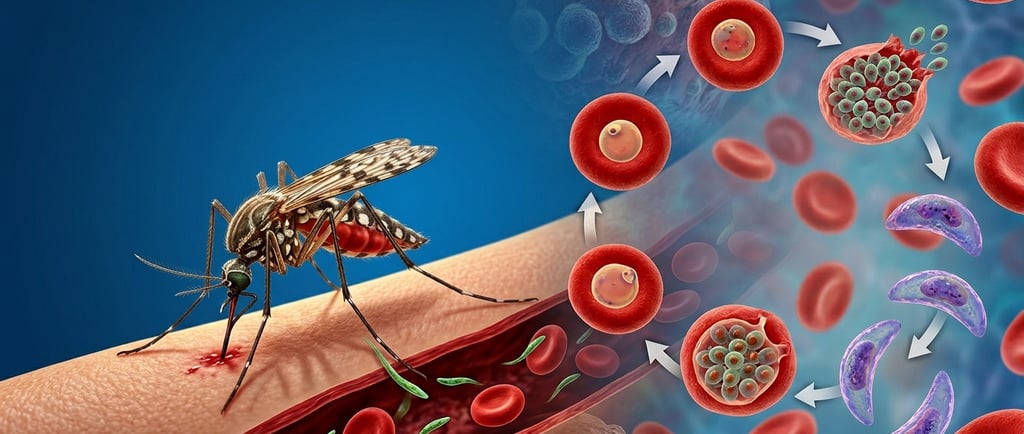
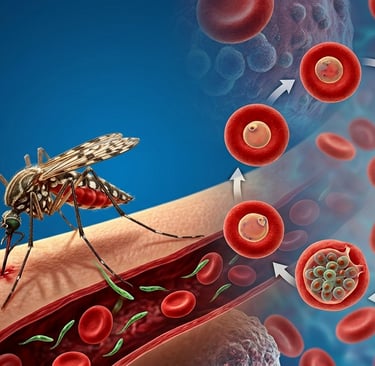
Desde el punto de vista biológico, el parásito presenta un ciclo de vida extraordinariamente sofisticado que alterna entre el huésped humano y el mosquito. Tras la inoculación, los esporozoitos migran rápidamente al hígado, donde invaden hepatocitos y se multiplican silenciosamente en forma de esquizontes hepáticos. Esta fase es clínicamente asintomática, pero crítica para la amplificación inicial del parásito. Posteriormente, miles de merozoitos son liberados al torrente sanguíneo, iniciando la fase eritrocitaria, responsable de la sintomatología clínica.
Una vez en la sangre, los merozoitos invaden los eritrocitos y comienzan un ciclo asexual intraeritrocitario que dura aproximadamente 24–48 horas dependiendo de la especie. Durante este proceso, el parásito pasa por diferentes estadios (anillo, trofozoito y esquizonte), replicándose activamente. La ruptura sincronizada de los eritrocitos infectados libera nuevos merozoitos y productos parasitarios que activan el sistema inmunológico, desencadenando la liberación de citocinas (como TNF-α, IFN-γ e IL-10), responsables de los episodios febriles característicos.
A nivel celular, la infección eritrocitaria induce profundas modificaciones estructurales y funcionales en los glóbulos rojos. El parásito remodela la membrana eritrocitaria, aumentando su rigidez y expresando proteínas de adhesión como PfEMP1, que permiten que los eritrocitos infectados se adhieran al endotelio vascular (citoadherencia). Este fenómeno evita su eliminación por el bazo, pero provoca obstrucción microvascular, especialmente en órganos críticos como el cerebro, contribuyendo al desarrollo de malaria grave o cerebral.
Además, el metabolismo del eritrocito se ve profundamente alterado para satisfacer las necesidades energéticas del parásito. Se incrementa el consumo de glucosa, la degradación de hemoglobina y la adquisición de nutrientes como el hierro. Estas alteraciones, junto con la destrucción masiva de eritrocitos infectados y no infectados, conducen a una de las complicaciones más frecuentes: la anemia malárica.
Desde una perspectiva clínica, los síntomas del paludismo reflejan directamente estos mecanismos fisiopatológicos. La fiebre periódica es consecuencia de la lisis sincronizada de eritrocitos, mientras que la anemia resulta de la hemólisis y de una eritropoyesis ineficaz. En casos graves, la citoadherencia y la inflamación sistémica pueden provocar complicaciones como malaria cerebral, acidosis metabólica, insuficiencia renal o síndrome de distrés respiratorio agudo.
Otro aspecto clave es la capacidad del parásito para evadir el sistema inmunitario. Plasmodium falciparum presenta una elevada variabilidad antigénica, especialmente en proteínas de superficie como PfEMP1, lo que dificulta el desarrollo de inmunidad esterilizante. Asimismo, algunas especies como P. vivax forman hipnozoitos en el hígado, capaces de reactivarse meses después de la infección inicial, perpetuando la enfermedad incluso en ausencia de nuevas picaduras.
Finalmente, una fracción de los parásitos en sangre se diferencia en gametocitos, las formas sexuales que pueden ser ingeridas por el mosquito durante una nueva picadura, cerrando así el ciclo de transmisión. En el mosquito, estos gametocitos sufren una transformación compleja que culmina en la formación de esporozoitos infecciosos en las glándulas salivales, listos para infectar a un nuevo huésped humano.
En conjunto, el paludismo no es simplemente una infección parasitaria, sino una enfermedad sistémica compleja en la que interactúan procesos inmunológicos, hematológicos y vasculares. La multiplicidad de fases del parásito y su capacidad de adaptación explican tanto la diversidad clínica como la dificultad para desarrollar intervenciones completamente eficaces.
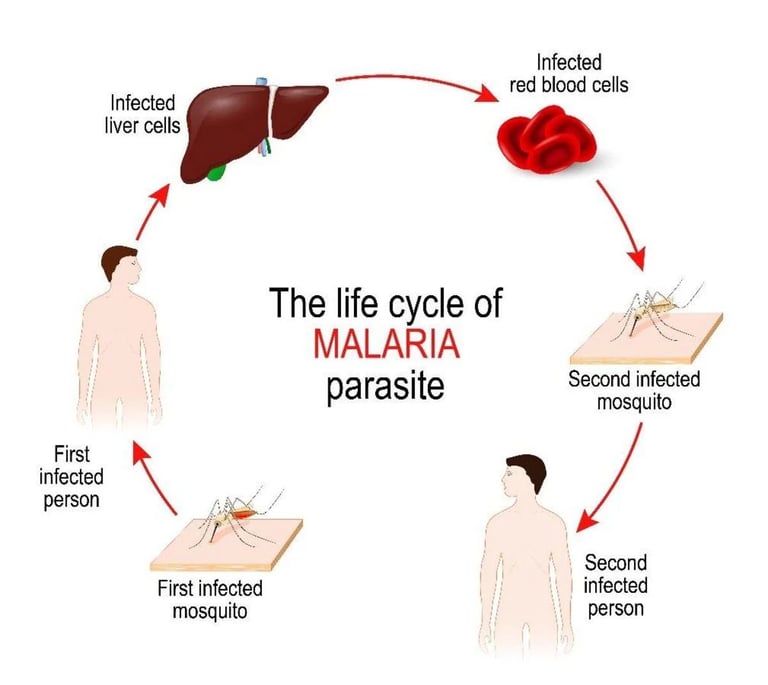
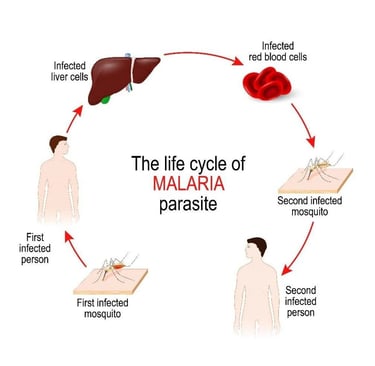
imagen: esquema general del ciclo de la malaria.
Fuente: horiba.com
Un problema global con epicentro en África
Es una realidad que, a día de hoy, el paludismo sigue siendo una enfermedad que golpea casi exclusivamente al continente africano. De hecho, si analizamos la situación global, nos daremos cuenta de que entre el 94 y el 95 por ciento de los casos y fallecimientos se concentran en el África subsahariana. Esta distribución tan marcada no es fruto del azar, por cierto; responde a una combinación de factores ecológicos que favorecen al mosquito y, sobre todo, a unas desigualdades socioeconómicas que no dejan de crecer.
Pero, sin duda, lo más doloroso es ponerle rostro a las cifras. Los niños menores de 5 años son los que sufren la peor parte, convirtiéndose en el grupo más frágil ante esta patología. Por ejemplo, en el año 2024, se estima que la malaria causó la muerte de unos 438.000 niños en la región africana.
A decir verdad, esta altísima mortalidad infantil tiene una explicación clara: la falta de una inmunidad adquirida lo suficientemente fuerte, sumada a un acceso muy limitado a los servicios de salud. Si a esto le añadimos los habituales retrasos en el diagnóstico, el resultado es una tragedia que se repite año tras año.
Sin embargo, el impacto no se queda solo en los hospitales. La carga económica que arrastra el paludismo es tan pesada que termina frenando el progreso de países enteros. Al reducir de forma drástica la productividad laboral y disparar el gasto sanitario, la enfermedad se encarga de perpetuar esos ciclos de pobreza de los que resulta tan difícil escapar. Al final, lo que es una crisis sanitaria acaba siendo un lastre que impide que estas sociedades puedan prosperar con normalidad.
¿Por qué sigue existiendo en pleno siglo XXI?
Si nos detenemos a analizarlo, la razón por la que el paludismo sigue tan presente entre nosotros no es solo una cuestión médica; de hecho, tiene muchísimo que ver con las profundas desigualdades estructurales que todavía arrastra la salud global. Es una realidad que en muchos países donde la enfermedad es endémica, los sistemas sanitarios no son lo suficientemente robustos, lo que supone un muro infranqueable a la hora de intentar aplicar estrategias de prevención o tratamientos que realmente funcionen a gran escala.
Cuando la infraestructura es precaria, algo tan vital como el acceso a diagnósticos rápidos o a un tratamiento adecuado se convierte en una auténtica odisea para la población. Sin embargo, no se trata solo de medicinas; incluso medidas preventivas que parecen sencillas, como el reparto de mosquiteras tratadas con insecticida, se vuelven muy difíciles de gestionar en estas condiciones.
Por si fuera poco, el contexto social no siempre ayuda. De hecho, los conflictos armados y las constantes crisis humanitarias no hacen más que agravar estas limitaciones, rompiendo cualquier pequeño avance que se haya logrado y dejando a las comunidades en una situación de desprotección total frente al parásito.
Por otro lado, no podemos ignorar que la naturaleza juega a favor de la enfermedad. Los factores climáticos son determinantes, ya que las condiciones específicas de temperatura y humedad son, por así decirlo, el caldo de cultivo ideal para la proliferación del mosquito vector.
A decir verdad, el panorama se complica aún más si miramos hacia el futuro. El cambio climático está alterando el tablero de juego, ya que está logrando ampliar las zonas geográficas donde el paludismo puede transmitirse. Básicamente, estamos viendo cómo el riesgo se extiende a territorios donde antes no existía, lo que nos obliga a replantearnos seriamente cómo frenar esta expansión.
Los grandes avances que han cambiado la lucha
En las últimas dos décadas, la lucha contra el paludismo ha experimentado una transformación significativa gracias a la combinación de estrategias preventivas, terapéuticas e innovaciones biomédicas. Estos avances no han eliminado la enfermedad, pero han logrado reducir sustancialmente la mortalidad y la morbilidad en múltiples regiones endémicas, especialmente en África subsahariana.
Uno de los pilares fundamentales ha sido la implementación masiva de mosquiteras impregnadas con insecticidas (ITNs). Estas redes actúan como una barrera física y química contra el mosquito Anopheles, reduciendo tanto el contacto humano-vector como la densidad de la población de mosquitos. Diversos estudios han demostrado que su uso sistemático puede reducir significativamente la incidencia de malaria clínica y la mortalidad infantil, convirtiéndose en una de las intervenciones más costo-efectivas en salud global.
En paralelo, el tratamiento farmacológico ha evolucionado de manera decisiva con la introducción de las terapias combinadas basadas en artemisinina (ACT). Estas combinaciones actúan rápidamente reduciendo la carga parasitaria y disminuyendo el riesgo de desarrollo de resistencias. Las ACT se han consolidado como el estándar terapéutico para malaria no complicada. Además, su uso ha contribuido a reducir la transmisión al disminuir la parasitemia circulante.
Otro avance relevante ha sido la mejora en las herramientas diagnósticas. Los tests rápidos de diagnóstico (RDTs) han permitido detectar la infección en entornos con recursos limitados sin necesidad de microscopía especializada. Esto ha facilitado el tratamiento precoz y ha reducido el uso innecesario de antimaláricos.
Sin embargo, el hito más significativo ha sido el desarrollo de las primeras vacunas eficaces. La vacuna RTS,S/AS01 (Mosquirix) representa el primer intento exitoso. Más recientemente, la vacuna R21/Matrix-M ha supuesto un salto cualitativo, con eficacias cercanas o superiores al 70–75% en la prevención de malaria clínica en niños.
A nivel inmunológico, estas vacunas se dirigen principalmente contra la proteína circunsporozoito del Plasmodium falciparum, bloqueando la infección en su fase hepática inicial. Aunque su eficacia disminuye con el tiempo, la administración de dosis de refuerzo ha demostrado mejorar significativamente la duración de la protección.
Además de las vacunas, se están desarrollando nuevas estrategias complementarias como la quimioprofilaxis estacional en niños, que consiste en la administración preventiva de antimaláricos durante las épocas de alta transmisión. Esta estrategia ha demostrado ser especialmente eficaz en regiones del Sahel.
Otro avance emergente es la aplicación de tecnologías genómicas para el control del vector. Entre ellas destacan las estrategias basadas en “gene drive” (impulso génico), que buscan modificar genéticamente las poblaciones de mosquitos para reducir su capacidad de transmitir el parásito.
En conjunto, estos avances han permitido reducir de forma notable la carga global del paludismo. Sin embargo, los progresos han comenzado a estancarse, lo que indica que las herramientas actuales no son suficientes por sí solas para lograr la erradicación.
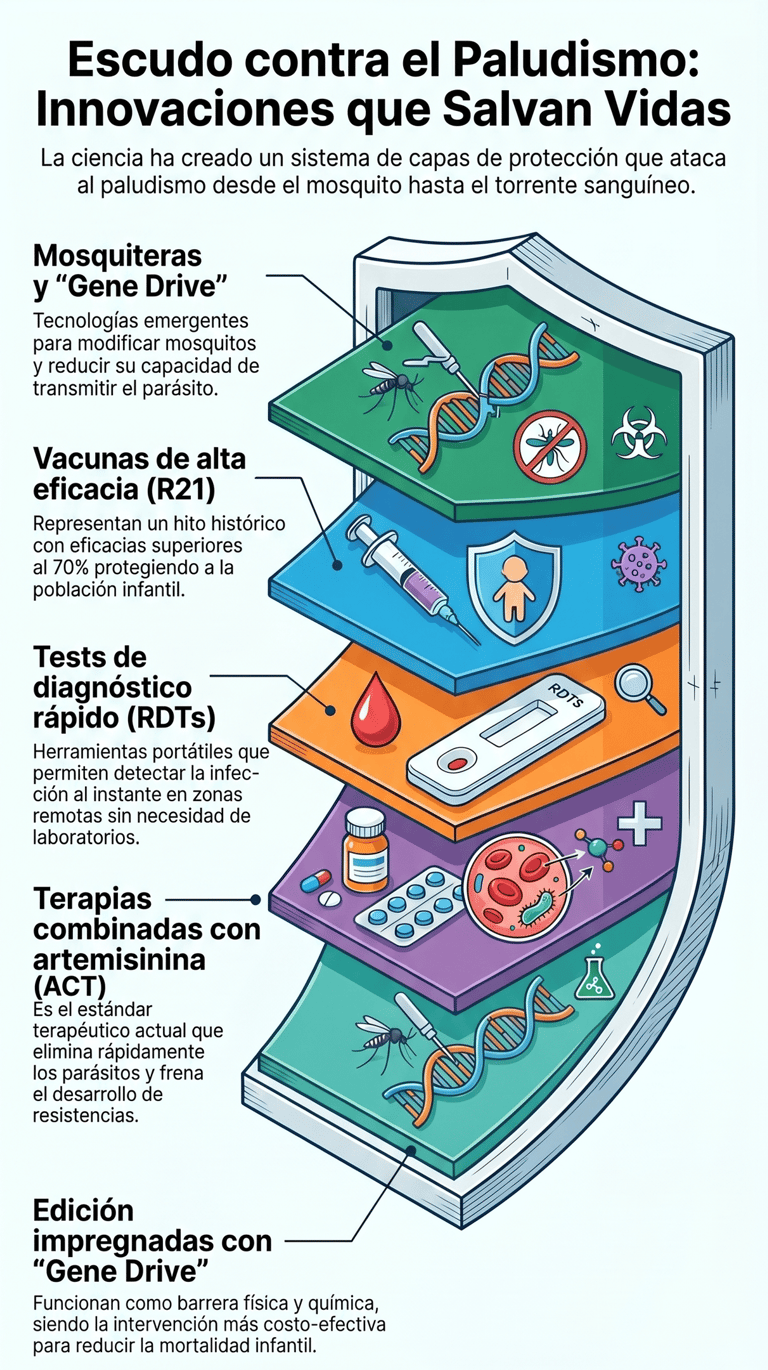
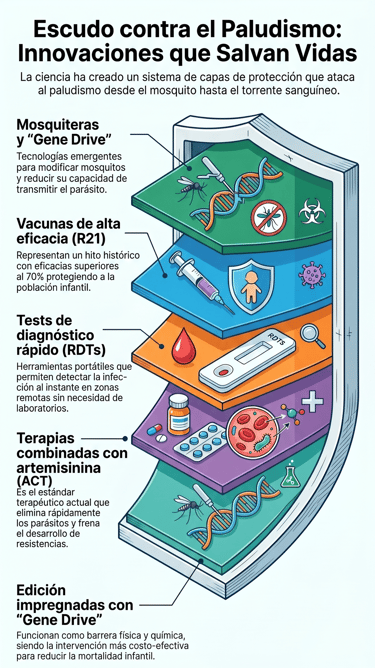
imagen: propia
Nuevas amenazas: resistencia y cambio climático: ¿Es posible erradicar la malaria?
Nos enfrentamos a un reto mayúsculo que pone en duda gran parte de lo que hemos logrado: la resistencia a los antimaláricos. Es un problema que empezó a documentarse en el sudeste asiático, pero que, por desgracia, ya está asomando la cabeza en África. La artemisinina, que ha sido nuestra gran aliada terapéutica durante años, ya no es tan infalible en esas zonas.
Por si fuera poco, no solo el parásito se está volviendo más fuerte; los mosquitos también están aprendiendo a defenderse. Se ha visto que están desarrollando una preocupante resistencia a los insecticidas, lo que hace que herramientas que antes eran fundamentales, como las mosquiteras, pierdan gran parte de su eficacia. De hecho, este fenómeno es una amenaza real que podría hacernos retroceder décadas en la lucha contra la enfermedad.
A decir verdad, el entorno tampoco ayuda. El cambio climático está alterando por completo los patrones de transmisión. Al cambiar las temperaturas y la humedad, el paludismo se está expandiendo hacia nuevas regiones que antes estaban totalmente libres de esta amenaza.
Sin embargo, no todo es pesimismo. Algunos países han conseguido eliminar el paludismo por completo, lo que nos demuestra que la erradicación es una meta alcanzable si se dan las circunstancias adecuadas. Eso sí, hay que ser realistas: estos casos de éxito suelen darse en lugares donde la carga inicial de la enfermedad era menor y donde ya contaban con infraestructuras sanitarias mucho más robustas.
Si nos paramos a pensar por qué no hemos ganado esta batalla todavía, la respuesta es una mezcla de ciencia y logística. Para empezar, la resistencia biológica y la enorme complejidad del ciclo del parásito hacen que sea un enemigo muy difícil de abatir. Además, no basta con actuar de forma puntual; se necesitan intervenciones sostenidas a largo plazo para que los resultados no se evaporen.
Por cierto, el gran cuello de botella sigue siendo el de siempre: la financiación global es insuficiente y la coordinación internacional todavía deja mucho que desear. Sin un flujo de recursos constante y una estrategia común, acabar con esta enfermedad seguirá siendo un objetivo lejano.
El futuro: innovación y desafíos
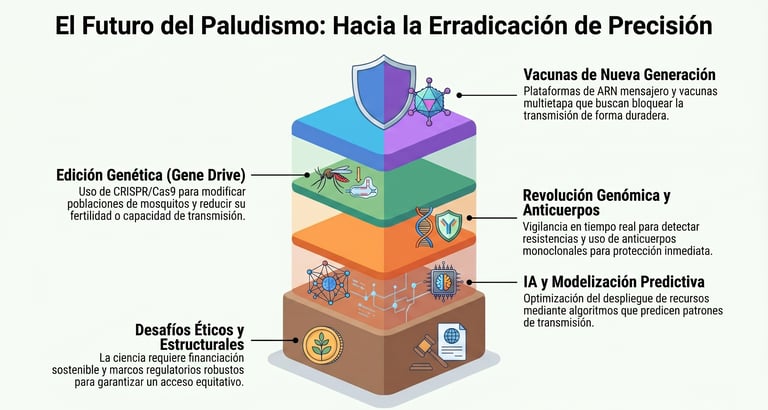
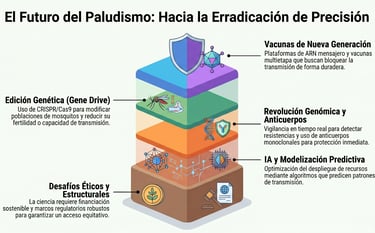
imagen: propia
El futuro del control y eventual erradicación del paludismo se encuentra en una fase de transición marcada por avances tecnológicos sin precedentes y, al mismo tiempo, por importantes incertidumbres científicas, éticas y operativas. La convergencia de disciplinas como la genómica, la biotecnología, la inteligencia artificial y la inmunología está redefiniendo el abordaje de esta enfermedad hacia enfoques de precisión.
Uno de los campos más prometedores es el desarrollo de nuevas generaciones de vacunas. La investigación se ha orientado hacia vacunas con mayor eficacia, duración y capacidad de bloquear la transmisión. Destacan plataformas innovadoras como las vacunas multietapa y tecnologías de ARN mensajero, que podrían superar la limitación de la inmunidad parcial y de corta duración.
Paralelamente, la inmunoprofilaxis mediante anticuerpos monoclonales está emergiendo como una alternativa para proporcionar protección inmediata en poblaciones de alto riesgo, complementando la vacunación tradicional.
Otro eje clave es la revolución genómica. El análisis del genoma ha permitido identificar dianas moleculares críticas. Además, la vigilancia genómica en tiempo real está facilitando la detección precoz de mutaciones asociadas a la resistencia, permitiendo una medicina de precisión aplicada a enfermedades infecciosas.
Sin embargo, la innovación más disruptiva es la edición genética, especialmente los sistemas basados en CRISPR/Cas9. Estas herramientas permiten modificar poblaciones de mosquitos mediante “gene drive” (impulso génico), favoreciendo la herencia preferencial de genes que reducen la capacidad de transmitir el parásito o disminuyen la fertilidad del vector. Esto podría traducirse en la supresión de poblaciones de Anopheles.
No obstante, estas tecnologías plantean desafíos éticos y ecológicos significativos. La liberación de organismos genéticamente modificados requiere marcos regulatorios robustos y consenso internacional debido a los posibles efectos impredecibles en los ecosistemas.
Otro ámbito emergente es el uso de inteligencia artificial y modelización avanzada para predecir patrones de transmisión y optimizar la distribución de recursos mediante modelos predictivos.
A pesar de estos avances, persisten desafíos estructurales como la financiación insuficiente, la desigualdad en el acceso y la debilidad de los sistemas sanitarios. El futuro no dependerá solo de la ciencia, sino de la capacidad global para integrar estas innovaciones en estrategias sostenibles y equitativas.
Conclusión
El paludismo no es solo un tema de medicina; es, ante todo, una afección que sigue echando raíces en las desigualdades globales. Aunque la ciencia no ha dejado de avanzar, que esta enfermedad persista con tanta fuerza pone en evidencia los fallos estructurales de nuestros sistemas de salud y la forma en que se reparten los recursos en el mundo actual.
La llegada de nuevas herramientas terapéuticas, como es el caso de las vacunas, ha abierto una ventana de esperanza real. De hecho, estos avances son fundamentales para reducir el impacto que la enfermedad tiene sobre la población vulnerable. Sin embargo, no debemos engañarnos pensando que son una solución mágica por sí solas. Para que funcionen, deben entenderse como una pieza más dentro de una estrategia integral mucho más amplia.
Técnicamente hablando, la erradicación del paludismo es algo posible, está a nuestro alcance. Pero, a decir verdad, para lograrlo se necesita algo más que buenos laboratorios: hace falta un compromiso sostenido a nivel mundial. Esto implica una inversión continua y, sobre todo, una hoja de ruta que ponga la equidad en el centro de todas las decisiones.
En resumidas cuentas, la malaria es mucho más que una simple enfermedad infecciosa. Hoy por hoy, funciona como un marcador muy claro de la desigualdad social, económica y sanitaria que todavía divide a nuestra sociedad contemporánea.

Referencias
· Abraham, I. C., Aboje, J. E., Ukoaka, B. M., et al. (2025). Integrating malaria vaccine and CRISPR/Cas9 gene drive: A comprehensive strategy for accelerated malaria eradication. Malaria Journal, 24(1), Artículo 17.
· Alghamdi, J. M., Al-Qahtani, A. A., Alhamlan, F. S., & Al-Qahtani, A. A. (2024). Recent advances in the treatment of malaria. Pharmaceutics, 16(11), 1416.
· Amaratunga, C., et al. (2022). Artemisinin resistance in Southeast Asia. The Lancet Infectious Diseases, 22(8), 1200–1215.
· Ashley, E. A., et al. (2022). Spread of artemisinin resistance in malaria. New England Journal of Medicine, 386(14), 1350–1362.
· Balmer, A. J., White, N. F. D., Ünlü, E. S., et al. (2025). Understanding the global rise of artemisinin resistance: Insights from over 100,000 Plasmodium falciparum samples. eLife, 14, e105544.
· Bhatt, S., et al. (2023). The effect of malaria control interventions on Plasmodium falciparum. Nature, 615(7952), 460–468.
· Bhattacharya, N., & Bhattacharya, A. (2024). First malaria vaccine RTS,S: A step toward the eradication of malaria. Cureus, 16(4), e58240.
· Birczyńska-Zych, M., Czepiel, J., Łabanowska, M., et al. (2023). Course of Plasmodium infection studied using 2D-COS on human erythrocytes. Malaria Journal, 22, Artículo 188.
· Björkman, A., & Morris, U. (2020). Why asymptomatic Plasmodium falciparum infections are common in low-transmission settings. Trends in Parasitology, 36(11), 898–905.
· Caminade, C., et al. (2023). Climate impacts on malaria distribution. Proceedings of the National Academy of Sciences (PNAS), 120(15), e2200111120.
· Duffy, P. E., & Gorres, J. P. (2024). Advances in malaria immunology and vaccine development. Nature Reviews Microbiology, 22(10), 620–635.
· Duffy, P. E., Gorres, J. P., Healy, S. A., & Fried, M. (2024). Malaria vaccines: A new era of prevention and control. Nature Reviews Microbiology, 22(12), 756–772.
· Dumarchey, A., Lavazec, C., & Verdier, F. (2022). Erythropoiesis and malaria: A multifaceted interplay. International Journal of Molecular Sciences, 23(21), 12762.
· Efficacy and immunogenicity of RTS,S/AS01 and R21/Matrix-M malaria vaccines: Systematic review and meta-analysis. (2026). Journal of Infection and Public Health. Publicación electrónica avanzada.
· Farmanpour Kalalagh, K., Rezaei, A., Hazrati, S., et al. (2025). Safeguarding artemisinin: Integrating bioproduction innovation and resistance management for malaria eradication. Malaria Journal, 24, Artículo 414.
· Fikadu, M., & Ashenafi, E. (2023). Malaria: An overview. Infection and Drug Resistance, 16, 3339–3347.
· Garrood, W. T., Cuber, P., Willis, K., et al. (2022). Driving down malaria transmission with engineered gene drives. Frontiers in Genetics, 13, Artículo 891218.
· Gething, P. W., et al. (2022). Climate change and malaria transmission. Nature Climate Change, 12(6), 520–530.
· Guttery, D. S., Zeeshan, M., Holder, A. A., & Tewari, R. (2024). The molecular mechanisms driving Plasmodium cell division. Biochemical Society Transactions, 52(2), 593–602.
· Hancock, P. A., North, A., Leach, A. W., et al. (2024). The potential of gene drives in malaria vector species to control malaria in African environments. Nature Communications, 15, Artículo 8976.
· Hemingway, J., et al. (2023). Vector control strategies for malaria. Annual Review of Entomology, 68, 420–440.
· Ménard, D., et al. (2023). Genetic basis of artemisinin resistance. Nature Communications, 14, Artículo 1250.
· Menkin-Smith, L., & Winders, W. T. (2023). Plasmodium vivax malaria. StatPearls Publishing.
· Mihreteab, S., et al. (2023). Increasing prevalence of artemisinin-resistant HRP2-negative malaria in Eritrea. New England Journal of Medicine, 389(13), 1191–1202.
· Naidoo, K., & Oliver, S. V. (2024). Gene drives: An alternative approach to malaria control? Human Genomics, 18(1), Artículo 22.
· Nature Communications Study Group. (2025). Malaria parasite remodeling of erythrocytes. Nature Communications, 16, Artículo 450.
· NEJM Review Authors. (2024). Malaria. New England Journal of Medicine, 390(15), 1420–1435.
· Noor, A. M., et al. (2022). Malaria risk mapping in Africa. The Lancet Global Health, 10(5), e650–e662.
· Olotu, A., et al. (2024). Safety and efficacy of R21/Matrix-M malaria vaccine in African children: Phase 3 trial. The Lancet, 403(10424), 333–344.
· Ouologuem, D. T., Dara, A., Kone, A., Ouattara, A., & Djimde, A. A. (2023). Plasmodium falciparum development from gametocyte to oocyst: Insight from functional studies. Microorganisms, 11(8), 1966.
· Oxford R21 Vaccine Group. (2023). Efficacy of R21/Matrix-M malaria vaccine. The Lancet, 401(10385), 1331–1341.
· Penny, M. A., et al. (2022). Modeling malaria eradication strategies. Nature Communications, 13, Artículo 2850.
· Rosenthal, P. J., Asua, V., & Conrad, M. D. (2024). Emergence, transmission dynamics and mechanisms of artemisinin partial resistance in malaria parasites in Africa. Nature Reviews Microbiology, 22(8), 490–505.
· RTS,S Clinical Trials Partnership. (2023). Efficacy and safety of RTS,S malaria vaccine. The Lancet, 401(10385), 1320–1330.
· Samuels, A. M., et al. (2022). Efficacy of RTS,S/AS01E malaria vaccine administered according to different regimens in children aged 5–17 months. The Lancet Infectious Diseases, 22(9), 1329–1342.
· Sherrard-Smith, E., et al. (2022). Mosquito resistance to insecticides. Nature Communications, 13, Artículo 3410.
· Siddiqui, A. J., Bhardwaj, J., Saxena, J., Jahan, S., Snoussi, M., Bardakci, F., Badraoui, R., & Adnan, M. (2023). A critical review on human malaria and schistosomiasis vaccines: Current state, recent advancements, and developments. Vaccines, 11(5), 920.
· Snow, R. W., et al. (2022). Global malaria burden and epidemiology. Nature, 602(7897), 420–428.
· Stanisic, D. I., & Good, M. F. (2023). Malaria vaccines: Progress to date. BioDrugs, 37(6), 737–756.
· StatPearls. (2023). Plasmodium falciparum malaria. StatPearls Publishing.
· Su, X., Stadler, R. V., Xu, F., & Wu, J. (2023). Malaria genomics, vaccine development, and microbiome. Pathogens, 12(8), 1061.
· Tinto, H., et al. (2023). Seasonal malaria vaccination strategies. The Lancet Infectious Diseases, 23(4), 450–462.
· Turan, G., Boggio, M. J., Othman, A. S., et al. (2026). Recent advances, bottlenecks, and future directions in Plasmodium falciparum vaccine development. Vaccines, 14(3), 277.
· Tusting, L. S., et al. (2022). Impact of insecticide-treated nets on malaria control. The Lancet Infectious Diseases, 22(6), 850–862.
· Watson, O. J., et al. (2024). Global risk of selection and spread of Plasmodium falciparum HRP2/3 gene deletions [Preprint]. medRxiv.
· Weiss, D. J., et al. (2023). Global malaria decline and resurgence trends. Nature, 618(7965), 550–558.
· White, N. J., et al. (2022). Malaria. The Lancet, 399(10336), 1710–1725.
· World Health Organization. (2023). World malaria report 2023. WHO Press.
· World Health Organization. (2024). Malaria vaccine implementation and recommendations.
· World Health Organization. (2026). Malaria vaccines (RTS,S and R21).
· World Health Organization Global Malaria Programme. (2024). Annual reports on malaria control 2022–2024.
· World Health Organization Malaria Vaccine Implementation Programme. (2024). RTS,S implementation outcomes.
· Wunderlich, J., Kotov, V., Votborg-Novél, L., Ntalla, C., Geffken, M., Peine, S., Portugal, S., & Strauss, J. (2024). Iron transport pathways in the human malaria parasite Plasmodium falciparum revealed by RNA-sequencing. Frontiers in Cellular and Infection Microbiology, 14, Artículo 1480076.