Párkinson: por qué no empieza con temblores y qué ocurre años antes del diagnóstico
José Hernández Jiménez
4/10/202618 min leer


1. Introducción
La enfermedad de Parkinson se ha consolidado como uno de los trastornos neurológicos con mayor impacto en todo el planeta. De hecho, su prevalencia ha crecido de una manera tan asombrosa en las últimas décadas que, hoy por hoy, su expansión es más veloz que la de cualquier otra patología de tipo neurodegenerativo. No es solo una estadística; es una realidad que afecta cada vez a más personas a nivel global.
Básicamente, este proceso progresivo se origina por una pérdida selectiva de neuronas dopaminérgicas. Estas células se encuentran en una región del cerebro conocida como sustancia negra y su desaparición es la que acaba provocando tanto las alteraciones motoras como las que no lo son.
Tradicionalmente, casi todos asociamos esta dolencia con el temblor en reposo, que es quizá su señal más conocida. Sin embargo, en los últimos años hemos aprendido que la historia empieza mucho antes. Por cierto, existen manifestaciones no motoras bastante sutiles que pueden aparecer años antes de que un médico dé el diagnóstico oficial.
Este cambio de visión ha sido clave. Gracias a ello, se ha impulsado una investigación mucho más profunda sobre las fases prodrómicas, la búsqueda de biomarcadores y nuevas formas de lograr un diagnóstico precoz que permita actuar lo antes posible.
Si nos asomamos al interior del cerebro desde un punto de vista fisiopatológico, lo que encontramos es una acumulación anómala de una proteína llamada alfa-sinucleína. Esta proteína se agrupa formando los conocidos cuerpos de Lewy, que van acompañados de esa degeneración progresiva de las neuronas que producen dopamina.
A pesar de que hemos avanzado muchísimo en entender cómo funciona la enfermedad a nivel molecular, lo cierto es que todavía queda camino por recorrer. A día de hoy, lamentablemente, aún no disponemos de una cura definitiva. Por eso, los enfoques médicos actuales se centran principalmente en ser tratamientos sintomáticos, buscando mejorar la calidad de vida de los pacientes mientras la ciencia sigue buscando la solución final.
2. El gran error: pensar que empieza con temblores
Mucha gente cree, de forma equivocada, que la enfermedad de Parkinson empieza siempre con un temblor en las manos. Sin embargo, lo cierto es que este es uno de los errores más extendidos sobre la patología. De hecho, diversas investigaciones han dejado claro que existe una fase prodrómica que puede arrancar muchísimos años antes de que aparezca cualquier problema de movimiento.
Durante este tiempo, el cuerpo lanza señales sutiles, conocidos como síntomas no motores, que a menudo pasamos por alto. Por cierto, hablamos de señales tan variadas como la depresión, el estreñimiento, la anosmia —que es la pérdida del sentido del olfato— o ciertos trastornos del sueño.
Uno de los predictores más potentes de las llamadas sinucleinopatías, categoría donde se incluye esta enfermedad, es el trastorno de conducta del sueño en fase de movimientos oculares rápidos. A pesar de su enorme valor diagnóstico, lo cierto es que en la práctica clínica diaria rara vez se utiliza para lograr un diagnóstico precoz.
El problema es que estos síntomas iniciales tienen una baja especificidad, lo que provoca que sean infradiagnosticados con frecuencia. Al final, se pierde una oportunidad de oro para intervenir antes de que el daño sea mayor.
El retraso diagnóstico no es un tema menor, ya que tiene consecuencias profundas. De hecho, se estima que para cuando los síntomas motores clásicos se hacen evidentes, el paciente ya ha perdido entre el 50% y el 60% de sus neuronas dopaminérgicas.
Esta realidad limita muchísimo la eficacia de las intervenciones neuroprotectoras, que tendrían un potencial mucho mayor si se aplicaran en las etapas iniciales. Por otro lado, los modelos científicos actuales sugieren que la neurodegeneración no empieza en el sistema nigroestriatal, como se pensaba antes. Curiosamente, parece que el proceso arranca fuera de ahí, posiblemente en el intestino o en el bulbo olfatorio, lo que explicaría por qué esos primeros síntomas no tienen nada que ver con el movimiento.
Afortunadamente, el reconocimiento de esta fase preclínica está cambiando las reglas del juego. Actualmente, se está poniendo mucho esfuerzo en el desarrollo de biomarcadores capaces de identificar cambios en las fases premotoras.
Sin duda, uno de los campos más prometedores es el uso de la inteligencia artificial, que está mostrando resultados muy esperanzadores para detectar la enfermedad mucho antes de lo que permiten los métodos tradicionales. Al final, el objetivo es claro: dejar de ir por detrás de la enfermedad y empezar a detectarla cuando todavía podemos proteger la mayor parte del cerebro.
3. ¿Qué es el Párkinson?
Cuando hablamos de la enfermedad de Parkinson, nos referimos a un trastorno de tipo neurodegenerativo bastante complejo que no aparece de la noche a la mañana. Todo empieza con una pérdida progresiva de esas células tan importantes llamadas neuronas dopaminérgicas, situadas en una zona muy específica del cerebro: la sustancia negra pars compacta.
Esta degradación provoca, en última instancia, que los niveles de dopamina en el cuerpo estriado caigan significativamente. Al final, este desequilibrio químico es el que termina por desbaratar el control motor de la persona, dificultando tareas que antes eran automáticas.
Si analizamos este proceso desde un ángulo histopatológico, hay un detalle que define perfectamente la patología. Se trata de la acumulación de alfa-sinucleína, una proteína que se agrupa de forma anómala para dar lugar a los conocidos cuerpos de Lewy.
Estas agrupaciones proteicas no son un simple residuo; de hecho, están directamente implicadas en la disfunción neuronal y en la posterior muerte celular. Es un proceso interno silencioso que marca la evolución de la enfermedad en cada paciente.
Es fundamental entender que la dopamina es la gran reguladora del movimiento. Por eso, cuando su presencia es deficiente, aparecen síntomas tan claros como la bradicinesia —esa lentitud tan característica—, la rigidez muscular y el temblor.
Sin embargo, la visión médica ha cambiado mucho recientemente. Hoy sabemos que este trastorno no es puramente dopaminérgico, ya que también se ven afectados otros sistemas neurotransmisores. Esta complejidad explica por qué los síntomas pueden ser tan variados entre una persona y otra.
Debido a esta enorme heterogeneidad clínica, la comunidad científica ha empezado a replantearse el concepto tradicional de la enfermedad. Actualmente, se prefiere verla como un síndrome complejo más que como una entidad única, reconociendo que existen múltiples subtipos biológicos y clínicos.
Por otro lado, las investigaciones más actuales han ampliado nuestro horizonte sobre los mecanismos que la provocan. Ahora se estudian a fondo procesos como la inflamación, el estrés oxidativo y la disfunción mitocondrial. Incluso se está prestando una atención increíble a las alteraciones del microbioma intestinal, lo que sugiere que la clave de lo que ocurre en el cerebro podría estar, en parte, en nuestro sistema digestivo.
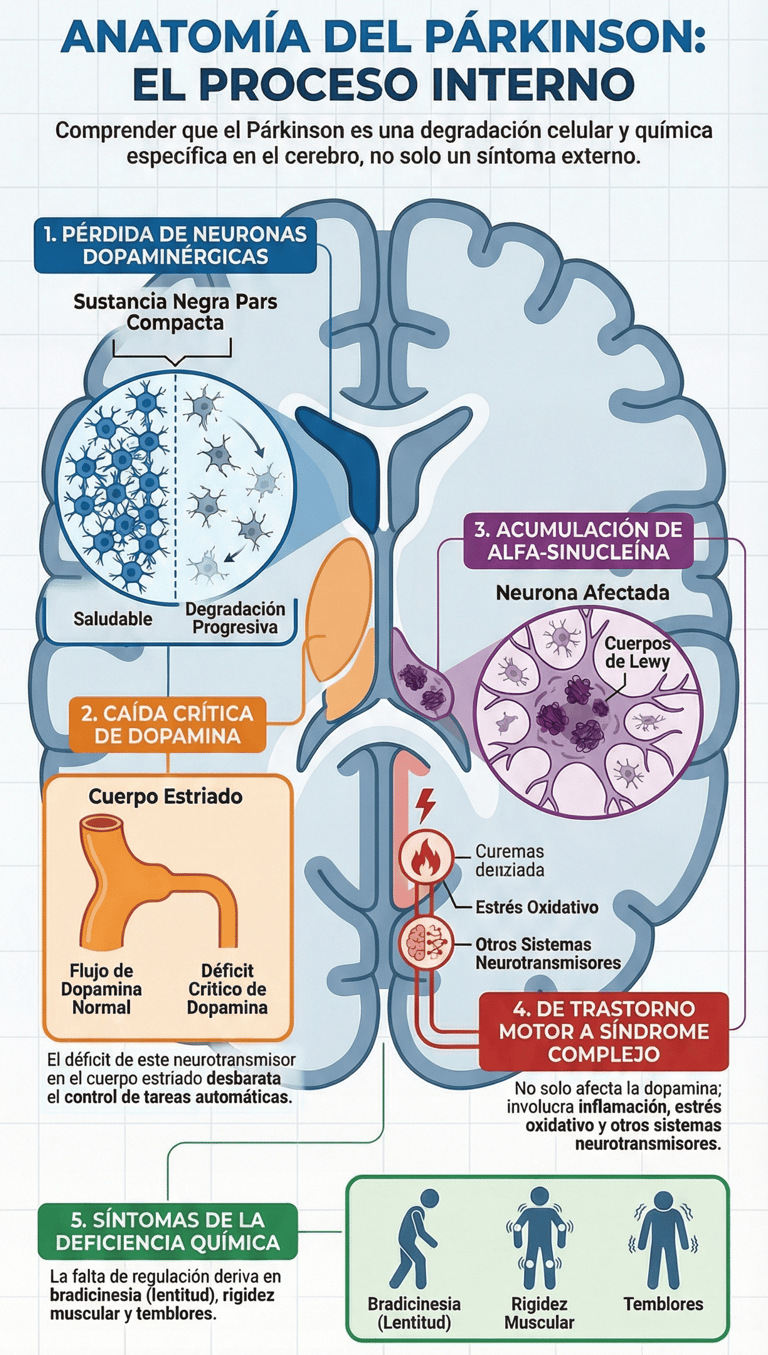
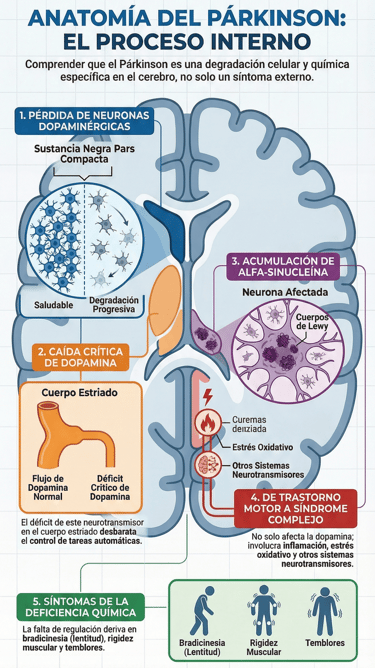
imagen: propia
4. Síntomas: mucho más que movimiento
Aunque los síntomas motores son los más visibles, la enfermedad de Parkinson incluye una amplia gama de manifestaciones no motoras que afectan significativamente la calidad de vida.
Síntomas motores
Algo que suele llamar mucho la atención al principio es que estas manifestaciones no aparecen de forma equilibrada en todo el cuerpo. Por lo general, los síntomas suelen ser asimétricos al inicio, lo que significa que es muy común empezar notando las molestias más en un lado que en el otro. Sin embargo, lo que realmente define este proceso es que las señales no son estáticas, sino que progresan con el tiempo de manera paulatina.
Entre los signos más característicos que se presentan, destaca la bradicinesia. Básicamente, se trata de esa lentitud de movimientos que tanto entorpece el día a día. A esto se le suma la rigidez muscular, que genera una tensión constante, y el conocido temblor en reposo, que suele ser el síntoma que más identifica el público general.
Con el avance de la situación, termina por aparecer la inestabilidad postural. Este factor es especialmente delicado, ya que afecta directamente al equilibrio y a la seguridad de la persona al caminar, cerrando así el círculo de los principales retos físicos a los que se enfrentan estos pacientes.
Síntomas no motores
A menudo, cuando pensamos en este tipo de condiciones, lo primero que nos viene a la mente son los problemas de movilidad. Sin embargo, lo cierto es que existe un conjunto de señales "invisibles" que van mucho más allá. A decir verdad, hablamos de situaciones tan complejas como la depresión, la ansiedad o diversos trastornos cognitivos.
De hecho, hay pacientes que lidian con dolor, alteraciones del sueño e incluso una disfunción autonómica que afecta a procesos internos del cuerpo. Lo más curioso es que estas molestias pueden preceder a los motores, apareciendo mucho antes que el primer temblor evidente. Por cierto, no hay que subestimarlos: para muchísimas personas, estos síntomas terminan siendo bastante más incapacitantes que la propia dificultad para moverse.
Últimamente, la evidencia científica ha dejado claro que el problema es mucho más profundo de lo que se creía tradicionalmente. Ya no se trata únicamente de una cuestión de falta de dopamina; ahora sabemos que estas manifestaciones están vinculadas a la afectación de múltiples sistemas neuroquímicos. Básicamente, el desajuste cerebral implica a diversas sustancias y no solo a los sistemas dopaminérgicos.
Por otro lado, hay que tener en cuenta que no existen dos casos idénticos. Existe una alta variabilidad interindividual, lo que significa que la forma en que la enfermedad da la cara en una persona puede ser totalmente distinta a como lo hace en otra. Sin duda, esta diversidad es lo que vuelve el manejo clínico un verdadero reto y hace que sea absolutamente necesario un enfoque personalizado. Al final, la medicina actual entiende que cada paciente necesita un plan diseñado específicamente para su realidad biológica.
5. ¿Por qué aparece?
La etiología de la enfermedad de Parkinson es multifactorial, con interacción entre factores genéticos y ambientales.
Genética
La ciencia, a través de la genética y la bioquímica, ha conseguido identificar algunos "culpables" moleculares en este proceso. De hecho, se ha comprobado que la presencia de mutaciones en genes muy concretos, como el LRRK2, el GBA o el SNCA, está estrechamente vinculada al desarrollo de la enfermedad de Parkinson.
Estas alteraciones genéticas no discriminan; por cierto, pueden "dar la cara" tanto en las llamadas formas familiares como en aquellas que surgen de manera esporádica en personas sin ningún tipo de antecedente previo.
Sin embargo, no debemos perder de vista la realidad estadística. A pesar de estos hallazgos tan importantes, lo habitual es que nos encontremos ante un escenario distinto. La gran mayoría de las situaciones clínicas actuales se siguen clasificando como casos idiopáticos, lo que significa que, en el fondo, su causa primaria todavía sigue siendo un misterio para los investigadores.
Factores ambientales
A decir verdad, no podemos mirar únicamente hacia el interior de nuestras células para entender por qué ocurre esto. La realidad es que el entorno en el que nos movemos tiene un peso considerable. De hecho, se ha comprobado que la exposición a pesticidas o el contacto con ciertos metales pesados son factores que no debemos perder de vista.
Del mismo modo, haber sufrido traumatismos craneales a lo largo de la vida puede dejar una huella importante. Por cierto, también se está estudiando con mucho interés cómo influyen ciertos elementos relacionados con nuestro microbioma intestinal, ya que parece que el equilibrio de nuestras bacterias internas dice mucho más de nuestra salud cerebral de lo que pensábamos.
Por otro lado, la ciencia está avanzando a pasos agigantados gracias a los estudios metabolómicos más recientes. Estas investigaciones han logrado poner nombre y apellidos a diversas alteraciones en vías metabólicas específicas, lo que nos da una pista fundamental. Al final, lo que estamos viendo es una interacción compleja en la que se mezclan la genética, el ambiente y nuestro propio metabolismo. No es una sola causa la que dispara el proceso, sino más bien un baile entre lo que heredamos, cómo vivimos y cómo funciona nuestra química interna.
Sin embargo, lo que realmente está centrando la atención de los expertos últimamente es la llamada hipótesis del eje intestino-cerebro. Esta idea ha cobrado una relevancia asombrosa, ya que plantea algo que antes nos parecería impensable: que el origen del problema podría no estar solo en la cabeza.
Básicamente, se sugiere que ciertos procesos inflamatorios periféricos —aquellos que ocurren fuera del cerebro— podrían ser el detonante que termine por desencadenar la neurodegeneración. Es decir, que una inflamación en otra parte del cuerpo podría acabar afectando a nuestras neuronas de forma irreversible.
6. Diagnóstico: retos actuales
El diagnóstico de esta afección sigue siendo fundamentalmente clínico. Esto significa que el médico se basa, sobre todo, en lo que ve durante la exploración, buscando señales claras como la bradicinesia —esa lentitud de movimientos tan característica— junto a otros síntomas motores.
Sin embargo, hay que reconocer que este método tiene sus límites, especialmente cuando la enfermedad está en sus etapas tempranas. De hecho, la precisión se complica porque existe una superposición con otros trastornos similares, lo que a veces hace que sea difícil distinguir una patología de otra al principio.
Un tema que genera mucho debate es que todavía no contamos con biomarcadores validados que se puedan usar de forma rutinaria en los hospitales. Aunque se han propuesto candidatos con mucho potencial, como la alfa-sinucleína, la proteína acídica fibrilar glial o distintos metabolitos, lo cierto es que ninguno ha funcionado lo suficientemente bien por sí solo.
A pesar de esto, no todo son malas noticias. Actualmente, está emergiendo una estrategia que promete cambiar las reglas del juego: el uso combinado de estos indicadores biológicos con herramientas de inteligencia artificial. Esta mezcla parece ser la vía más clara para lograr una detección precoz que realmente marque la diferencia para el paciente.
Por otro lado, contamos con el apoyo de técnicas de neuroimagen avanzada, como las tomografías por emisión de positrones o de fotones y la resonancia magnética. Estas herramientas son fascinantes porque permiten a los especialistas evaluar disfunciones neurotransmisoras y observar cambios estructurales en el cerebro que no se ven a simple vista.
Sin embargo, conviene recordar que, a pesar de lo avanzadas que son, su uso sigue considerándose complementario. Al final, la tecnología ayuda a confirmar sospechas y a dar seguridad, pero la evaluación directa de los síntomas sigue siendo el pilar principal para entender qué le está pasando a la persona.
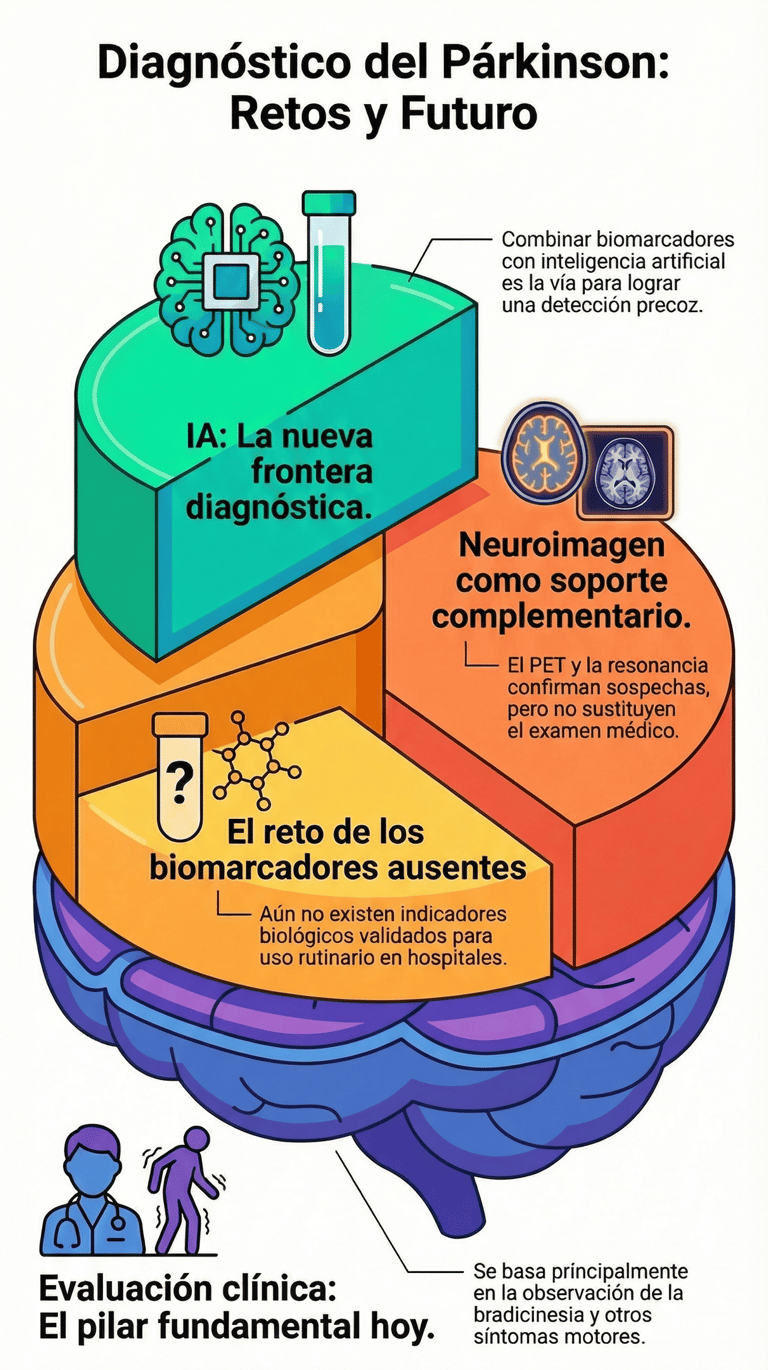
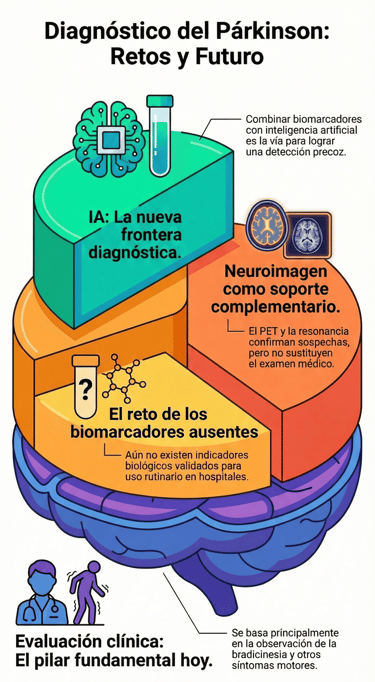
imagen: propia
7. Tratamientos actuales
El enfoque médico para tratar la enfermedad de Parkinson se centra casi exclusivamente en el control sintomático. Lo que se busca, básicamente, es aliviar las molestias diarias para que la persona pueda mantener su calidad de vida el mayor tiempo posible.
En este escenario, la levodopa sigue siendo la herramienta más potente y eficaz que tenemos a nuestra disposición, ya que su función principal es restaurar los niveles de dopamina en el cerebro. Sin embargo, no es una solución exenta de problemas. Por cierto, hay que tener en cuenta que, cuando se utiliza de forma prolongada, es muy habitual que empiecen a surgir diversas complicaciones motoras que dificultan el manejo del paciente.
Más allá de los fármacos, la rehabilitación juega un papel que es, sencillamente, fundamental. No se trata solo de ir a una sesión puntual, sino de integrar la fisioterapia, la terapia ocupacional y el ejercicio físico como parte de la rutina. Al final, estos pilares son los que permiten que el paciente mantenga su funcionalidad y pueda seguir valiéndose por sí mismo en las tareas más cotidianas.
Para aquellos casos que ya se encuentran en etapas más avanzadas, la medicina ofrece alternativas como la estimulación cerebral profunda. Es una técnica fascinante porque, según indican investigaciones recientes, no solo ayuda a controlar los síntomas, sino que también podría estar influyendo de manera positiva en los biomarcadores de neuroplasticidad.
Sin embargo, hay que ser realistas. A pesar de todos estos avances y de lo mucho que hemos mejorado en la gestión de los síntomas, todavía no contamos con ningún tratamiento que sea capaz de modificar de forma significativa la progresión de la enfermedad. Seguimos trabajando para encontrar esa llave que, en el futuro, nos permita frenar el avance del proceso degenerativo.
8. El futuro del Párkinson
El futuro de la enfermedad de Parkinson está dando un giro radical hacia lo que hoy conocemos como medicina de precisión. Ya no hablamos de soluciones genéricas; de hecho, el objetivo ahora es adaptar cada intervención a la realidad biológica de cada individuo.
Dentro de este nuevo abanico de posibilidades, están surgiendo opciones realmente prometedoras. Por ejemplo, se está trabajando intensamente en la inmunoterapia dirigida específicamente contra la alfa-sinucleína, así como en innovadoras terapias génicas y diversas estrategias neuroprotectoras que buscan, por encima de todo, frenar el daño en el sistema nervioso.
La inteligencia artificial está provocando una auténtica revolución en la forma en que detectamos la patología. Gracias a su capacidad para procesar biomarcadores complejos, ahora podemos interpretar datos digitales que antes pasaban desapercibidos.
Por cierto, gran parte de este avance se debe a herramientas que ya forman parte de nuestra vida, como los sensores y los dispositivos móviles. Estos aparatos no son solo gadgets; son fuentes de información constante que permiten identificar patrones sutiles en la salud del paciente.
Este uso de la tecnología nos lleva a los denominados biomarcadores digitales. Lo más interesante de estas herramientas es que permiten monitorizar la evolución de la situación en tiempo real. Sin duda, esto supone un salto cualitativo, ya que facilita una personalización del tratamiento mucho más fina y reactiva.
Sin embargo, el verdadero potencial reside en la suma de todas las partes. El enfoque que viene no se quedará solo en un dato aislado; probablemente combinará datos genéticos, bioquímicos, clínicos y digitales. Al final, el objetivo es lograr una caracterización más precisa de cada paciente, entendiendo que cada caso es único y requiere una respuesta a su medida.
9. Conclusión
Es curioso cómo ha cambiado nuestra visión sobre la enfermedad de Parkinson en los últimos años. De hecho, hemos dejado atrás esa idea de que se trata de un simple trastorno motor para entenderla como lo que realmente es: una enfermedad multisistémica compleja. Este cambio de concepto no es solo teórico; ha transformado por completo la manera en la que los especialistas se enfrentan a ella, entendiendo que afecta al organismo de una forma mucho más global de lo que pensábamos.
Uno de los puntos clave en este nuevo enfoque es el reconocimiento de la fase prodrómica. Ahora sabemos que la importancia de los síntomas no motores es vital para entender cómo empieza todo. Sin embargo, aquí es donde nos encontramos con una piedra en el camino. A pesar de que el enfoque diagnóstico ha evolucionado muchísimo, todavía sufrimos limitaciones importantes. El motivo principal es que aún nos falta contar con biomarcadores validados que nos den una respuesta clara y definitiva en las consultas del día a día.
Afortunadamente, no todo son obstáculos. De hecho, los avances en campos como la neuroimagen y la metabolómica, sumados al potencial de la inteligencia artificial, están dibujando un futuro muy distinto. Estas herramientas están abriendo puertas que antes estaban cerradas, permitiéndonos soñar con un diagnóstico precoz y, sobre todo, con una medicina personalizada que se adapte a las necesidades biológicas de cada individuo, y no a soluciones generales.
Sin embargo, hay que ser realistas: el principal reto sigue siendo la ausencia de terapias modificadoras de la enfermedad. Es decir, tratamientos que no solo alivien, sino que cambien el destino del proceso. Por eso, el esfuerzo de la investigación futura debe volcarse sin descanso en las intervenciones tempranas y en el desarrollo de estrategias neuroprotectoras que pongan un freno real al daño celular.
En definitiva, estamos ante un campo que se mueve a una velocidad asombrosa. Aunque los pasos que se están dando son muy prometedores, lo cierto es que todavía resultan insuficientes para cambiar de forma radical el curso de la enfermedad. Estamos en el camino, pero aún queda mucho por descubrir.

10. Referencias
Aarsland, D., Tanavia, A. S., Larsen, J. P., & Ballard, C. (2023). Cognitive decline in Parkinson disease. Nature Reviews Neurology, 19(1), 21–34.
Armstrong, M. J., & Okun, M. S. (2023). Diagnosis and treatment of Parkinson disease: A review. JAMA, 323(6), 548–560.
Arya, R., et al. (2024). Parkinson's disease: Biomarkers for diagnosis and disease progression. International Journal of Molecular Sciences, 25(22), 12379.
Athauda, D., & Foltynie, T. (2022). The ongoing pursuit of neuroprotective therapies in Parkinson disease. Nature Reviews Neurology, 18(1), 25–40.
Bandres-Ciga, S., et al. (2023). Genetics in Parkinson’s disease: Current state and future directions. Movement Disorders, 38(2), 184–196.
Berg, D., et al. (2022). Prodromal Parkinson disease. Nature Reviews Neurology, 18(1), 9–23.
Billingsley, K. J., et al. (2023). Genetic architecture of Parkinson’s disease. Nature Reviews Genetics, 24(3), 158–174.
Blauwendraat, C., et al. (2022). Genetics of Parkinson disease. Nature Reviews Neurology, 18(3), 170–184.
Blesa, J., et al. (2022). Oxidative stress in Parkinson disease: Looking for the elusive link. Frontiers in Neuroanatomy, 16, 845552.
Bloem, B. R., Okun, M. S., & Klein, C. (2022). Parkinson’s disease. The Lancet Neurology, 397(10291), 2284–2303.
Brooker, S. M., & Gonzalez-Latapi, P. (2025). Biomarkers in Parkinson's disease. Neurologic Clinics, 43(2), 229–248.
Brundin, P., et al. (2022). α-synuclein propagation: From Western blots to Parkinson’s disease. Nature Reviews Molecular Cell Biology, 23(4), 241–256.
Chaudhuri, K. R., et al. (2023). Non-motor symptoms of Parkinson disease: Diagnosis and management. Nature Reviews Neurology, 19(5), 259–275.
Chen, X., et al. (2023). α-synuclein pathology in Parkinson disease: From biology to bedside. Acta Neuropathologica, 145(1), 1–18.
Das, S., & Ramteke, H. (2024). A comprehensive review of the role of biomarkers in early diagnosis of Parkinson’s disease. Cureus, 16(3), e55921.
Dauer, W., & Przedborski, S. (2022). Parkinson disease: Mechanisms and models. Neuron, 110(3), 432–449.
Deng, H., et al. (2022). The role of genetics in Parkinson's disease. Neuroscience Bulletin, 38(2), 213–228.
Deuschl, G., et al. (2023). DBS in Parkinson disease: A review of current practices. Movement Disorders, 38(4), 512–525.
Dorsey, E. R., et al. (2022). Global burden of Parkinson disease: A call to action. The Lancet Neurology, 21(12), 1071–1072.
Eshuis, S. A., et al. (2022). Diagnostic imaging in Parkinson disease. Journal of Neurology, 269(6), 2845–2860.
Espay, A. J., et al. (2023a). Disease modification in Parkinson disease: A review. JAMA Neurology, 80(2), 115–124.
Espay, A. J., et al. (2023b). Precision medicine in Parkinson disease. Nature Reviews Neurology, 19(4), 211–222.
Espay, A. J., et al. (2024). Revisiting disease-modifying strategies in Parkinson disease. Movement Disorders, 39(1), 5–15.
Feigin, V. L., et al. (2023). Global epidemiology of Parkinson disease. Lancet Public Health, 8(4), e243–e254.
Heim, B., et al. (2023). Neuroimaging advances in Parkinson disease. Brain, 146(2), 438–452.
Heinzel, S., et al. (2022). Update of the MDS research criteria for prodromal Parkinson's disease. Movement Disorders, 37(8), 1592–1605.
Hirsch, E. C., et al. (2023). Neuroinflammation in Parkinson disease: A review. Nature Reviews Neurology, 19(3), 145–160.
Houser, M. C., & Tansey, M. G. (2022). The gut-brain axis in Parkinson disease. Nature Reviews Neurology, 18(2), 89–106.
Iranzo, A., et al. (2023). REM sleep behavior disorder and Parkinson disease. The Lancet Neurology, 22(1), 60–72.
Kalia, L. V., & Lang, A. E. (2022). Parkinson's disease. The Lancet, 399(10321), 165–179.
Kalia, L. V., et al. (2023). Clinical heterogeneity of Parkinson disease. Nature Reviews Neurology, 19(6), 337–351.
Little, S., et al. (2022). Adaptive deep brain stimulation for Parkinson’s disease. Brain, 145(3), 809–821.
Lozano, A. M., et al. (2022). Deep brain stimulation in Parkinson disease. Nature Reviews Neurology, 18(4), 204–220.
McNamara, A., Carr, L. M., Baetu, I., Jenkinson, M., & Collins-Praino, L. (2026). Towards a biologically defined diagnosis: Incorporating pathophysiological measures into Parkinson's disease clinical criteria. Parkinson’s Disease, 2026, Article 41757373.
Mollenhauer, B., et al. (2022). Fluid biomarkers in Parkinson disease. The Lancet Neurology, 21(11), 1018–1032.
Nalls, M. A., et al. (2022). Genetic risk factors in Parkinson disease. The Lancet Neurology, 21(6), 551–564.
Oertel, W., et al. (2023). Recent advances in Parkinson’s disease therapy. Journal of Neural Transmission, 130(3), 321–335.
Parkinson disease therapy: current strategies and future research priorities. (2024). Nature Reviews Neurology, 20(11), 643–658.
Parra, J. C., et al. (2024). AI in Parkinson disease diagnosis. npj Parkinson's Disease, 10(1), 1–12.
Poewe, W., et al. (2022). Parkinson disease. Nature Reviews Disease Primers, 8(1), 1–21.
Poewe, W., et al. (2023). Pathophysiology of Parkinson disease. Nature Reviews Neurology, 19(2), 71–86.
Politis, M. (2023). Neuroimaging in Parkinson disease. Nature Reviews Neurology, 19(7), 395–410.
Postuma, R. B., et al. (2022). Identifying prodromal Parkinson’s disease. Movement Disorders, 37(6), 1111–1123.
Rovini, E., et al. (2023). Wearable sensors in Parkinson disease: A systematic review. Sensors, 23(2), 654.
Sardi, S. P., et al. (2023). GBA mutations and Parkinson disease: From biology to clinics. Neuron, 111(5), 650–664.
Schapira, A. H. V., et al. (2022). Novel therapies for Parkinson’s disease. The Lancet Neurology, 21(8), 733–744.
Scheperjans, F., et al. (2022). Gut microbiota in Parkinson disease. Nature Reviews Neurology, 18(7), 385–399.
Schneider, S. A., & Alcalay, R. N. (2023). Neuropathology of Parkinson disease. The Lancet Neurology, 22(10), 945–956.
Sharma, P., & Dhamija, R. K. (2025). The quest for Parkinson's disease biomarkers: Traditional and emerging multi-omics approaches. Molecular Biology Reports, 52(1), 145.
Singleton, A. B., et al. (2022). The genetic landscape of Parkinson’s disease. Nature, 605(7911), 621–631.
Stoker, T. B., & Barker, R. A. (2023). Recent developments in the treatment of Parkinson's disease. F1000Research, 12, 1–15.
Strafella, A. P., et al. (2022). Imaging biomarkers in Parkinson disease. The Lancet Neurology, 21(4), 365–376.
Subramaniam, S. R., & Chesselet, M. F. (2022). Mitochondrial dysfunction in Parkinson disease. Progress in Neurobiology, 213, 102262.
Surmeier, D. J., et al. (2022). Dopamine neuron vulnerability in Parkinson’s disease. Neuron, 110(11), 1735–1750.
Tansey, M. G., et al. (2022). Inflammation in Parkinson disease: A review. Nature Reviews Immunology, 22(11), 657–673.
Tolosa, E., Poewe, W., Noyce, A. J., Svenningsson, P., Mahlknecht, P., & Martí, M. J. (2026). Towards biomarker-based diagnosis of Parkinson disease. Nature Reviews Neurology, 22(1), 12–28.
Tuominen, R. K., & Renko, J. M. (2024). Biomarkers of Parkinson's disease in perspective of early diagnosis and translation of neurotrophic therapies. Basic & Clinical Pharmacology & Toxicology, 134(2), 145–158.
Visanji, N. P., et al. (2023). Biomarker discovery in Parkinson disease. Movement Disorders, 38(3), 365–378.
Weingarten, C. P., et al. (2022). Imaging in prodromal Parkinson disease. Movement Disorders, 37(9), 1785–1798.
World Health Organization. (2022). Parkinson disease: A public health approach.